10.实验是研究化学的基础,下列有关实验的方法、装置或操作都正确的是( )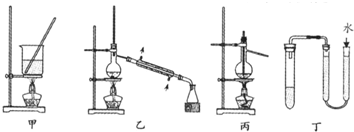

| A. | 用甲装置将海带灼烧成灰 | |
| B. | 分离Na2CO3溶液和CH3COOC2H5,可使用如图乙所示实验装置 | |
| C. | 利用丙装置进行石油分馏 | |
| D. | 利用丁装置检验装置的气密性 |
9.X、Y、Z三种元素的原子,其最外层电子排布分别为3s1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式为( )
| A. | X2YZ3 | B. | XYZ2 | C. | X2YZ2 | D. | XYZ3 |
8.下列化学用语的书写正确的是( )
| A. | 基态Mg原子的核外电子排布图: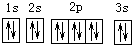 | |
| B. | 过氧化氢的电子式: | |
| C. | As原子的简化电子排布式:[Ar]4s24p3 | |
| D. | 羟基的电子式: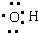 |
7.按电子排布,可以把周期表中的元素划分成几个区( )
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
4.某校化学兴趣小组对以下三种品牌牙膏中摩擦剂成分进行调查,结果如表.
试回答下列问题:
(1)上述三种摩擦剂中属于酸性氧化物的是SiO2(填化学式,下同);既能与强酸反应又能与强碱反应的是Al(OH)3.
(2)两面针儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
(3)从摩擦剂成分考虑,向珍珠防臭牙膏样品中滴加少量稀盐酸,可观察到的现象是有气泡生成,该反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O.
(4)中华透明牙膏摩擦剂SiO2是工业制备晶体硅的原料,其反应原理是SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO(用化学反应方程式表示).
(5)若制取珍珠防臭牙膏的原料碳酸钙中混入了少量铝粉,应加入试剂NaOH溶液进行除杂,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
| 牙膏品牌 | 两面针儿童牙膏 | 珍珠防臭牙膏 | 中华透明牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(1)上述三种摩擦剂中属于酸性氧化物的是SiO2(填化学式,下同);既能与强酸反应又能与强碱反应的是Al(OH)3.
(2)两面针儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
(3)从摩擦剂成分考虑,向珍珠防臭牙膏样品中滴加少量稀盐酸,可观察到的现象是有气泡生成,该反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O.
(4)中华透明牙膏摩擦剂SiO2是工业制备晶体硅的原料,其反应原理是SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO(用化学反应方程式表示).
(5)若制取珍珠防臭牙膏的原料碳酸钙中混入了少量铝粉,应加入试剂NaOH溶液进行除杂,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
3.下列有关离子检验的操作和实验结论正确的是( )
| A. | 向某溶液加入NaOH并微热,产生能够使湿润的红色石蕊试纸变蓝的无色气体,该溶液中一定含有NH4+ | |
| B. | 向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,该溶液中一定含有SO42- | |
| C. | 向某溶液中加入氨水,产生白色沉淀,则该溶液中一定含有Mg2+ | |
| D. | 用铂丝蘸取某溶液在酒精灯火焰上灼烧,若火焰呈黄色,则证明该溶液中无K+离子 |
2.下列生活小常识或家庭小实验中不涉及化学变化的是( )
| A. | 用食醋去除水垢 | |
| B. | 用竹炭包可清楚衣柜内的异味 | |
| C. | 用铁钉等材料探究铁生锈的条件 | |
| D. | 用柠檬汁涂抹在切开苹果表面可防止苹果变色 |
1.材料与化学密切相关.下列物质与用途对应关系不正确的是( )
0 153363 153371 153377 153381 153387 153389 153393 153399 153401 153407 153413 153417 153419 153423 153429 153431 153437 153441 153443 153447 153449 153453 153455 153457 153458 153459 153461 153462 153463 153465 153467 153471 153473 153477 153479 153483 153489 153491 153497 153501 153503 153507 153513 153519 153521 153527 153531 153533 153539 153543 153549 153557 203614
| A. | 碘化钾--加碘盐 | B. | 氧化铝--耐火材料 | ||
| C. | 铁碳合金--碳素钢 | D. | 硅酸盐--普通玻璃 |