题目内容
10.实验是研究化学的基础,下列有关实验的方法、装置或操作都正确的是( )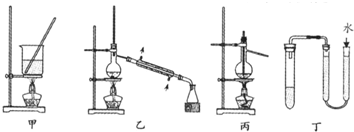
| A. | 用甲装置将海带灼烧成灰 | |
| B. | 分离Na2CO3溶液和CH3COOC2H5,可使用如图乙所示实验装置 | |
| C. | 利用丙装置进行石油分馏 | |
| D. | 利用丁装置检验装置的气密性 |
分析 A.灼烧固体应用坩埚;
B.CH3COOC2H5不溶于水;
C.温度计不能插入液面以下;
D.能形成压强差的装置能检验装置气密性.
解答 解:A.灼烧固体应用坩埚,蒸发液体用蒸发皿,故A错误;
B.CH3COOC2H5不溶于水,应用分液分离,故B错误;
C.温度计不能插入液面以下,应与蒸馏烧瓶支管口处,故C错误;
D.该装置中乙中两管液体能形成压强差,可以根据左边管中液体高度是否变化检验装置气密性,故D正确.
故选D.
点评 本题考查实验方案设计,为高考高频点,涉及物质分离、气密性检验等知识点,明确物质性质、基本实验操作原理即可看到,会从反应原理、物质性质、基本操作的规范性进行评价,题目难度不大.

练习册系列答案
相关题目
20.下列说法中错误的是( )
| A. | 淀粉、纤维素和蛋白质均属于高分子化合物 | |
| B. | 用漂白粉漂白时,向水溶液中加几滴白醋,会增强漂白效果 | |
| C. | 利用乙醇的还原性以及Cr3+、Cr2O7-的颜色差异来检验酒后驾车 | |
| D. | 合成纤维和光导纤维都是新型无机非金属材料 |
15.标准状况下,将15.68LCO2与500mL2mol/L的NaOH溶液充分反应,生成了Na2CO3和NaHCO3,再将溶液蒸干充分灼烧,得到的固体物质质量为( )
| A. | 84g | B. | 65.4g | C. | 67.6g | D. | 53g |
2.某研究性学习小组设计如图装置制取氯气并检验氯气的某些性质.
(1)制取Cl2,检验干燥氯气是否有漂白性.
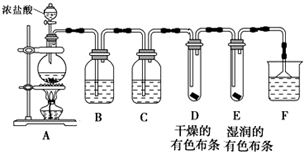
①盛装浓盐酸的仪器的名称是分液漏斗,烧瓶中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
②B中盛有饱和食盐水,其作用是除去Cl2中混有的HCl,C中盛装的试剂是浓硫酸
③通入Cl2后,D、E中观察到的现象是中布条不褪色,E中布条褪色;根据现象可得出的结论是干燥的Cl2没有漂白性.
④F中盛有NaOH溶液,其作用是吸收氯气,防止环境污染,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为0.1mol.
(2)探究铁丝在Cl2中燃烧的产物
某同学认为,当足量Cl2与少量铁丝反应时生成FeCl3,当少量Cl2与足量铁丝反应时生成FeCl2.为检验该观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物配制成溶液A、B,并取溶液进行以下实验,请填写下表中的空格.
④根据实验结论,铁丝在Cl2中点燃的化学方程式:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3 .
(1)制取Cl2,检验干燥氯气是否有漂白性.

①盛装浓盐酸的仪器的名称是分液漏斗,烧瓶中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
②B中盛有饱和食盐水,其作用是除去Cl2中混有的HCl,C中盛装的试剂是浓硫酸
③通入Cl2后,D、E中观察到的现象是中布条不褪色,E中布条褪色;根据现象可得出的结论是干燥的Cl2没有漂白性.
④F中盛有NaOH溶液,其作用是吸收氯气,防止环境污染,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为0.1mol.
(2)探究铁丝在Cl2中燃烧的产物
某同学认为,当足量Cl2与少量铁丝反应时生成FeCl3,当少量Cl2与足量铁丝反应时生成FeCl2.为检验该观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物配制成溶液A、B,并取溶液进行以下实验,请填写下表中的空格.
| 实验方法 | 实验现象 | 结论 |
| 分别向A、B溶液中滴加2滴①KSCN溶液 | ②两份溶液都变血红色 | 生成物中都有FeCl3 |
| 分别向A、B溶液中滴加几滴KMnO4溶液 | 两份溶液颜色均无明显变化 | 生成物中都不含③FeCl2 |
19.NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.0 L 1.0 mol•L-1的NaAlO2水溶液中含有的氧原子数为2 NA? | |
| B. | 常温下,0.l mol碳酸钠晶体中含有CO32- 的个数为0.1NA | |
| C. | 标准状况下,11.2L 18O2中所含中子数为8NA | |
| D. | 25℃时,l L pH=13的Ba(OH)2溶液中含有的OH- 数为0.2 NA |
20.硅及其化合物的应用范围很广.下列说法正确的是( )
| A. | 硅是人类将太阳能转换为电能的常用材料 | |
| B. | 单质硅是制光导纤维的材料 | |
| C. | 粗硅制备高纯度单质硅不涉及氧化还原反应 | |
| D. | 硅能与氢氟酸反应,则硅可以与盐酸反应 |
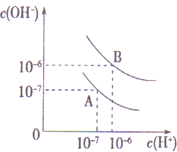 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: