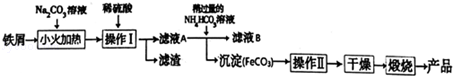
10.分子式为C4H10O的醇和C4H8O2的羧酸所形成的酯有(不包括立体异构)( )
| A. | 4种 | B. | 16种 | C. | 8种 | D. | 12种 |
5.化学与生活密切相关,下列说法不正确的是( )
| A. | 甘油可作护肤保湿剂 | |
| B. | 无水氯化钙可用作食品干燥剂 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱 |
4.在密闭容器中进行反应:H2(g)+Br2(g)?2HBr(g)△H<0,达到平衡后,欲使颜色加深,应采取的措施是( )
| A. | 升高温度 | B. | 使用催化剂 | C. | 增大H2浓度 | D. | 减小压强 |
3.氢氧燃料电池以氢气作还原剂,氧气作氧化剂,电极为多孔镍,电解质溶液为30%的氢氧化钾溶液.下列说法正取的是( )
| A. | 负极反应为:O2+2H2O+4e-═4OH- | |
| B. | 负极反应为:2H2+4OH--4e-═4H2O | |
| C. | 电池工作时溶液中的阴离子移向正极 | |
| D. | 电池工作时负极区pH升高,正极区pH下降 |
2. “C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.
“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.
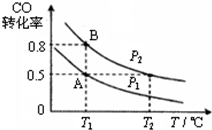
(1)向体积为 2L的密闭容器中充入1mol CO和2mol H2,在一定条件下发生如下反应:CO(g)+2H2(g)?CH3OH(g).经过t秒达到平衡,平衡时CO的转化率与温度、压强的关系如图所示.请回答:
①p1、T1℃时,从开始到平衡的过程中,用H2表示的平均反应速率为$\frac{0.5}{t}$mol•L-1•s-1
②图中压强p1< 压强p2.(填“>”、“<”或“=”)
(2)一定温度下,在三个体积均为 1.0L的恒容密闭容器中发生如下反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)
①容器I中反应达到平衡所需时间比容器Ⅲ中的短(填“长”、“短”或“相等”)
②达到平衡时,容器I中的CH3OH的体积分数相等(填“大于”、“小于”或“相等”)容器Ⅱ中的CH3OH的体积分数.
③若起始时向容器I中充入CH3OH 0.1mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向正反应方向进行(填“正反应”、“逆反应”或“不移动”).
(3)一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).若反应在恒容绝热(不
与外界交换能量)条件下进行,按下表数据投料,反应达到平衡状态,测得体系压强升高.
则升高温度,该反应的平衡常数将减小(填“增大”“减小”或“不变”).
 “C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.
“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.(1)向体积为 2L的密闭容器中充入1mol CO和2mol H2,在一定条件下发生如下反应:CO(g)+2H2(g)?CH3OH(g).经过t秒达到平衡,平衡时CO的转化率与温度、压强的关系如图所示.请回答:
①p1、T1℃时,从开始到平衡的过程中,用H2表示的平均反应速率为$\frac{0.5}{t}$mol•L-1•s-1
②图中压强p1< 压强p2.(填“>”、“<”或“=”)
(2)一定温度下,在三个体积均为 1.0L的恒容密闭容器中发生如下反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)
| 容器 编号 | 温度(℃) | 起始的物质的量(mol) | 平衡的物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
②达到平衡时,容器I中的CH3OH的体积分数相等(填“大于”、“小于”或“相等”)容器Ⅱ中的CH3OH的体积分数.
③若起始时向容器I中充入CH3OH 0.1mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向正反应方向进行(填“正反应”、“逆反应”或“不移动”).
(3)一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).若反应在恒容绝热(不
与外界交换能量)条件下进行,按下表数据投料,反应达到平衡状态,测得体系压强升高.
| 物质 | CO2 | H2 | CH3OH | H2O |
| 起始投料/mol | 1 | 3 | 2 | 0 |
1.利用如图所示装置(电极均为惰性电极) 可吸收SO2,并制取硫酸和烧碱溶液,下列说法正确的是( )
0 153359 153367 153373 153377 153383 153385 153389 153395 153397 153403 153409 153413 153415 153419 153425 153427 153433 153437 153439 153443 153445 153449 153451 153453 153454 153455 153457 153458 153459 153461 153463 153467 153469 153473 153475 153479 153485 153487 153493 153497 153499 153503 153509 153515 153517 153523 153527 153529 153535 153539 153545 153553 203614

| A. | 气体W为氧气 | |
| B. | b极与电源的正极相连 | |
| C. | 离子交换膜c为阳离子交换膜 | |
| D. | a极的电极反应为SO2+2H2O-2e-=SO42-+4H+. |