1.下列有机物命名正确的是( )
| A. | CH3-CH═CH-CH3 二丁烯 | B. | 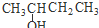 2-羟基丁烷 2-羟基丁烷 | ||
| C. | CH3OOCC2H5 乙酸乙酯 | D. | CH3CH(CH3)CH2COOH 3-甲基丁酸 |
20.在相同的A、B密闭容器中分别充入2mol SO2和1mol O2,使它们在一定温度下反应,并达新平衡:2SO2+O2
?2SO3(g).若A容器保持体积不变,B容器保持压强不变.当A中SO2的转化率为25%时,B中SO2的转化率为( )
?2SO3(g).若A容器保持体积不变,B容器保持压强不变.当A中SO2的转化率为25%时,B中SO2的转化率为( )
| A. | 25% | B. | 大于25% | C. | 小于25% | D. | 无法判断 |
19.一种新型燃料电池,它是用两根金属做电极插入KOH溶液中,然后向两极上分别通入甲烷和氧气,其电极反应为:X极:CH4+10OH--8e-═CO32-+7H2O,Y极:4H2O+2O2+8e-═8OH-,关于此燃料电池的有关说法错误的是( )
| A. | X为负极、Y为正极 | |
| B. | 工作一段时间后,KOH的物质的量不变 | |
| C. | 在标况下通过5.6 L O2完全反应则有l.0 mol 电子发生转移 | |
| D. | 该电池工作时甲烷一极附近溶液 pH降低 |
17.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁均有水珠 | 两种物质均受热分解 |
| B | 向某溶液中滴加氯水后再加入KSCN溶液 | 溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结. | NH4Cl固体可以升华 |
| A. | A | B. | B | C. | C | D. | D |
16.铁上镀铜时,电镀池的阴极为( )
| A. | 铜 | B. | 金 | C. | 石墨 | D. | 铁 |
15.合成氨是基本无机化工,氨是化肥工业和有机化工的主要原料,也是一种常用的制冷剂.
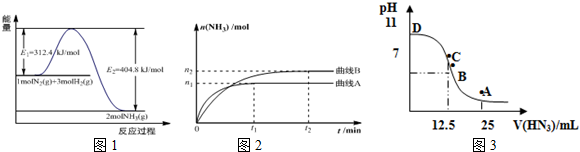
(1)图1是合成氨反应的能量与反应过程相关图(未使用催化剂);图2是合成氨反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图.
①下列说法正确的是BDE.
A.使用催化剂会使E1的数值增大
B.△H=-92.4kJ•mol-1
C.为了提高转化率,工业生产中反应的温度越低越好
D.在曲线A条件下,反应从开始到平衡,消耗N2的平均速率为$\frac{{n}_{1}}{4{t}_{1}}$mol•L-1•min-1
E.该反应的平衡常数KA<KB
F.图2是不同压强下反应体系中氨的物质的量与反应时间关系图,且PA<PB
②下列能说明该反应达到平衡状态的是D
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.v正(N2)=v逆(H2)
C.混合气体的密度保持不变
D.容器内压强保持不变
(2)合成氨技术的创立开辟了人工固氮的重要途径,合成氨反应的平衡常数K值和温度的关系如下:
400°C时,测得某时刻氨气、氮气、氢气的物质的量浓度分别为3mol•L-1、2mol•L-1、1mol•L-1时,此时刻该反应的v逆(N2)>v正(N2) (填“>”、“<”或“=”).
(3)常温下向25mL0.1mol/LNH3•H2O 溶液中,逐滴加入 0.2mol/L的HN3溶液,溶液的pH变化曲线如图3所示.
A、B、C、D 四个点中,水的电离程度最大的是C;A点时溶液中各离子浓度由小到大的顺序为c(OH-)<c(H+)<c(NH4+)<c(N3-).
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造新型燃料电池.试写出该电池的正极反应式N2+8H++6e-═2NH4+.

(1)图1是合成氨反应的能量与反应过程相关图(未使用催化剂);图2是合成氨反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图.
①下列说法正确的是BDE.
A.使用催化剂会使E1的数值增大
B.△H=-92.4kJ•mol-1
C.为了提高转化率,工业生产中反应的温度越低越好
D.在曲线A条件下,反应从开始到平衡,消耗N2的平均速率为$\frac{{n}_{1}}{4{t}_{1}}$mol•L-1•min-1
E.该反应的平衡常数KA<KB
F.图2是不同压强下反应体系中氨的物质的量与反应时间关系图,且PA<PB
②下列能说明该反应达到平衡状态的是D
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.v正(N2)=v逆(H2)
C.混合气体的密度保持不变
D.容器内压强保持不变
(2)合成氨技术的创立开辟了人工固氮的重要途径,合成氨反应的平衡常数K值和温度的关系如下:
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
(3)常温下向25mL0.1mol/LNH3•H2O 溶液中,逐滴加入 0.2mol/L的HN3溶液,溶液的pH变化曲线如图3所示.
A、B、C、D 四个点中,水的电离程度最大的是C;A点时溶液中各离子浓度由小到大的顺序为c(OH-)<c(H+)<c(NH4+)<c(N3-).
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造新型燃料电池.试写出该电池的正极反应式N2+8H++6e-═2NH4+.
14.用石墨作电极电解4mol•L-1的 CuSO4溶液,当c(Cu2+)为0.1mol•L-1时,停止电解,向剩余溶液中加入下列何种物质可使电解质溶液恢复至原来状态( )
| A. | Cu(OH)2 | B. | CuSO4•5H2O | C. | CuSO4 | D. | CuO |
13.某蓄电池放电、充电时的反应为Fe+Ni2O3+3H2O  Fe(OH)2+2Ni(OH)2下列推断中不正确的是( )
Fe(OH)2+2Ni(OH)2下列推断中不正确的是( )
①放电时,Fe为正极,Ni2O3为负极
②充电时,阴极上的电极反应式是Fe(OH)2+2e-═Fe+2OH-
③充电时,Ni(OH)2为阳极
④蓄电池的电极必须是浸在某种碱性电解质溶液中.
0 153327 153335 153341 153345 153351 153353 153357 153363 153365 153371 153377 153381 153383 153387 153393 153395 153401 153405 153407 153411 153413 153417 153419 153421 153422 153423 153425 153426 153427 153429 153431 153435 153437 153441 153443 153447 153453 153455 153461 153465 153467 153471 153477 153483 153485 153491 153495 153497 153503 153507 153513 153521 203614
 Fe(OH)2+2Ni(OH)2下列推断中不正确的是( )
Fe(OH)2+2Ni(OH)2下列推断中不正确的是( )①放电时,Fe为正极,Ni2O3为负极
②充电时,阴极上的电极反应式是Fe(OH)2+2e-═Fe+2OH-
③充电时,Ni(OH)2为阳极
④蓄电池的电极必须是浸在某种碱性电解质溶液中.
| A. | ① | B. | ①②④ | C. | ①③④ | D. | ②③④ |