18.将 0.1L 含有 0.02mol CuSO4 和 0.01molNaCl 的水溶液用惰性电极电解.电解一段时间后,一个电极上得到 0.01mol Cu,另一电极析出的气体( )
| A. | 只有 Cl2 | B. | 既有 Cl2 又有 O2 | ||
| C. | 只有 O2 | D. | 只有 H2 |
17.已知热化学方程式:2SO2(g)+O2(g)?2SO3(g); H=-Q kJ•mol-1(Q>0).下列说法 正确的是( )
| A. | 相同条件下,2 mol SO2(g)和 1 mol O2(g)所具有的能量小于 2 mol SO3(g)所具有的能量 | |
| B. | 将 2 mol SO2(g)和 1 mol O2(g)置于一密闭容器中充分反应后,放出热量为 Q kJ | |
| C. | 增大压强或升高温度,该平衡都向逆反应方向移动 | |
| D. | 如将一定量 SO2(g)和 O2(g)置于某密闭容器中充分反应放热 Q kJ,则此过程中有 2 mol SO2(g)被氧化 |
16.目前常用的镍(Ni)镉(Cd)电池,在现代生活中有广泛应用,它的充放电反应按下式进行Cd+2NiO(OH)+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2由此可知,该电池放电时的负极是( )
| A. | Cd(OH)2 | B. | Cd(OH)2 | C. | Cd | D. | NiO(OH) |
15.用1.000mol/LNaOH溶液滴定0.100mol/LH2SeO3溶液,在下图曲线标注位置,下面什么物质含硒量最少占溶液中硒总量的10%.( )
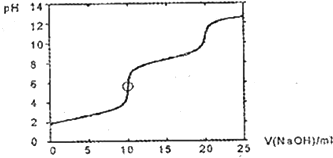

| A. | H2SeO3 | B. | H2SeO3和HSeO3- | C. | HSeO3- | D. | HSeO3-和SeO32- |
14.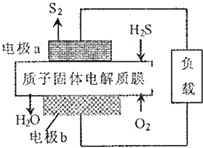 H2S利用是回收能最并得到单质硫.反应原理为:2H2S(g)+02(g)═S2(s)+2H20(1)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池示意图.下列说法正确的是( )
H2S利用是回收能最并得到单质硫.反应原理为:2H2S(g)+02(g)═S2(s)+2H20(1)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池示意图.下列说法正确的是( )
 H2S利用是回收能最并得到单质硫.反应原理为:2H2S(g)+02(g)═S2(s)+2H20(1)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池示意图.下列说法正确的是( )
H2S利用是回收能最并得到单质硫.反应原理为:2H2S(g)+02(g)═S2(s)+2H20(1)△H=-632kJ•mol-1.下图为质子膜H2S燃料电池示意图.下列说法正确的是( )| A. | 该电池可实现把化学能全部转化为电能 | |
| B. | 电极b上发生的电极反应为:02+2H2O+4e-═40H- | |
| C. | 电极a上发生的电极反应为:2H2S-4e-═S2+4H+ | |
| D. | 当有34gH2S参与反应时,有2mo1H+经质子膜进人负极区 |
13.实验室欲用Na2CO3•10H20晶体配制1mol/L的Na2CO3溶液100mL,下列说法正确的是( )
| A. | 要完成实验需称取10.6gNa2CO3•10H20晶体 | |
| B. | 本实验需用到的仪器只有药匙、玻璃棒、烧杯、胶头滴管和100 mL容量瓶 | |
| C. | 配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 | |
| D. | 定容时用胶头滴管滴人的蒸馏水滴在容量瓶内部刻度线上方会导致浓度偏低 |
12.下列物质互为同分异构体的是( )
| A. | 12C与13C | B. | O2与O3 | C. | 苯与甲苯 | D. | 1-丙醇与2-丙醇 |
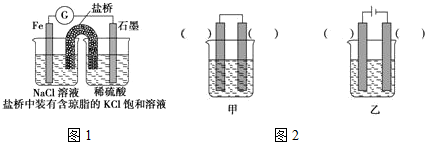
10.有关下列装置的叙述不正确的是( )
0 153265 153273 153279 153283 153289 153291 153295 153301 153303 153309 153315 153319 153321 153325 153331 153333 153339 153343 153345 153349 153351 153355 153357 153359 153360 153361 153363 153364 153365 153367 153369 153373 153375 153379 153381 153385 153391 153393 153399 153403 153405 153409 153415 153421 153423 153429 153433 153435 153441 153445 153451 153459 203614
| A. | 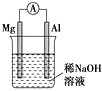 图铝片发生的电极反应式是:Al+4OH-3e-═AlO2-+2H2O | |
| B. |  图发生析氢腐蚀,离子反应方程式为:Fe+2H+═Fe2++H2↑ | |
| C. | 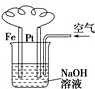 图溶液中发生了变化:4Fe(OH)2+O2+2H2O═4Fe(OH)3 | |
| D. | 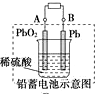 图充电时,阳极反应是:PbSO4+2H2O-2e-═=PbO2+SO42-+4H+ |
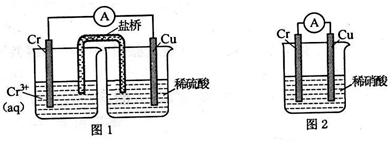 铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各 种性能的不锈钢,CrO3大量地用于电镀工业中.
铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各 种性能的不锈钢,CrO3大量地用于电镀工业中.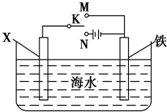 ,可以模拟铁的电化学防护.若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于N处.若 X 为锌,开关K 置于N或M处.
,可以模拟铁的电化学防护.若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于N处.若 X 为锌,开关K 置于N或M处.