6.科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空.如图1所示装置中,以稀土金属材料做惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-离子(O2+4e→2O2-).下列说法不正确的是( )


| A. | c电极的名称为正极,d电极上的电极反应式为CH4-8e-+4O2-═CO2+2H2O | |
| B. | 如图2所示,a电极上的电极反应式为4OH--4e-═2H2O+O2↑ | |
| C. | 如图2所示电解100mL0.5mol/LCuSO4溶液,若a电极产生56mL(标准状况)气体,则所得溶液的pH=1(不考虑溶液体积变化) | |
| D. | 若要使电解质溶液恢复到电解前的状态,可加入Cu2(OH)2CO3 |
5.如图所示,装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图.装置(Ⅰ)的离子交换膜只允许Na+通过.已知电池充、放反应的化学方程式为 2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr.当闭合开关K时,X极上有红色物质析出,下列说法正确的是( )
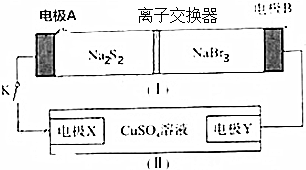

| A. | 装置①中钠离子从右到左通过离子交换膜 | |
| B. | B极的电极反应式为NaBr3+2e-+2Na═3NaBr | |
| C. | X电极的电极反应式为2Cl--2e-═Cl2↑ | |
| D. | 每有0.1mol Na+通过离子交换膜,X电极上析出固体物质0.64g |
4.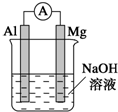 将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )
将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )
 将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )
将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )| A. | Mg比Al活泼,Mg失去电子被氧化成Mg2+ | |
| B. | 铝条表面虽有氧化膜,但可不必处理 | |
| C. | 正极反应式为2H++2e-═H2↑ | |
| D. | Al是电池负极,开始工作时溶液中会立即有白色沉淀析出 |
3.一澄清透明的溶液中,已知各离子的浓度相等,可能含有的阳离子有Na+、Fe2+、Ba2+、NH4+,可能含有的阴离子有Cl-、NO3-、CO32-、SO42-.向该混合溶液中加足量稀盐酸,有无色气体生成,且阴离子的种类不变.下列叙述正确的是( )
| A. | 该溶液-定含有Fe2+、Cl-、NO3- | B. | 该溶液一定不含Na+、NH4+、SO42- | ||
| C. | 该无色气体对环境无污染 | D. | 该溶液可能含有Ba2+ |
19. 氮元素在地球上丰度较大,氮及其化合物用途广泛.请回答:
氮元素在地球上丰度较大,氮及其化合物用途广泛.请回答:
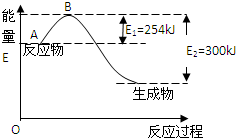
(1)如图是氮气和氢气反应生成1mol氨气的能量变化示意图,写出上述反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol
(2)已知下列数据:
根据表中和图中数据,计算N-H的键能为:390 kJ/mol
(3)用氨催化还原NOx(氮氧化物),可消除污染.
已知:4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H1=-a kJ/mol
N2(g)+O2(g)═2NO(g)△H2=-b kJ/mol
则反应:4NH3(g)+6NO(g)═5N2(g)+6H2O(g) 的反应热△H=-(a+3b)kJ/mol (用含a和b的代数式表示)其中氧化剂是NO,还原剂是NH3(均填分子式)
0 153226 153234 153240 153244 153250 153252 153256 153262 153264 153270 153276 153280 153282 153286 153292 153294 153300 153304 153306 153310 153312 153316 153318 153320 153321 153322 153324 153325 153326 153328 153330 153334 153336 153340 153342 153346 153352 153354 153360 153364 153366 153370 153376 153382 153384 153390 153394 153396 153402 153406 153412 153420 203614
 氮元素在地球上丰度较大,氮及其化合物用途广泛.请回答:
氮元素在地球上丰度较大,氮及其化合物用途广泛.请回答:(1)如图是氮气和氢气反应生成1mol氨气的能量变化示意图,写出上述反应的热化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol
(2)已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/( kJ/mol) | 435 | 943 |
(3)用氨催化还原NOx(氮氧化物),可消除污染.
已知:4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H1=-a kJ/mol
N2(g)+O2(g)═2NO(g)△H2=-b kJ/mol
则反应:4NH3(g)+6NO(g)═5N2(g)+6H2O(g) 的反应热△H=-(a+3b)kJ/mol (用含a和b的代数式表示)其中氧化剂是NO,还原剂是NH3(均填分子式)
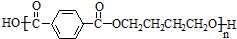
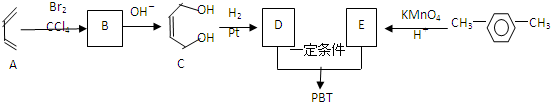
 互为同系物关系.
互为同系物关系.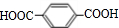 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$