题目内容
1.已知某实验室用水煤气合成甘(乙)氨酸的流程如下:
已知:R-CN $\stackrel{H_{2}O/H}{→}$ R-COOH 反应④属于加成反应.回答:
(1)写出A→B的化学方程式:2CH3OH+O2$→_{△}^{Cu}$2HCHO+2H2O,指出其反应类型氧化反应
(2)比较沸点高低:A>B 主要原因是:甲醇分子间存在氢键
(3)写出C→D的化学方程式:CH2=NH+HCN→H2N-CH2-CH2
(4)任写一种甘氨酸的同分异构体的结构简式:CH3CH2NO2 或 HO-CH2CONH2 等
2分子甘氨酸形成一种二肽的结构简式:H2NCH2CONHCH2COOH.
分析 A为CH3OH,在Cu作催化剂、加热条件下氧化生成B为HCHO,B与氨气分子脱去1分子水生成CH2=NH2,CH2=NH2与HCN发生加成反应生成D,D水解得到甘氨酸(H2NCH2COOH),则D为H2NCH2CN,据此解答.
解答 解:A为CH3OH,在Cu作催化剂、加热条件下氧化生成B为HCHO,B与氨气分子脱去1分子水生成CH2=NH2,CH2=NH2与HCN发生加成反应生成D,D水解得到甘氨酸(H2NCH2COOH),则D为H2NCH2CN.
(1)A→B的化学方程式:2CH3OH+O2$→_{△}^{Cu}$2HCHO+2H2O,其反应类型为氧化反应,
故答案为:2CH3OH+O2$→_{△}^{Cu}$2HCHO+2H2O;氧化反应;
(2)甲醇分子间存在氢键,则沸点甲醇>甲醛,
故答案为:>;甲醇分子间存在氢键;
(3)C→D的化学方程式:CH2=NH+HCN→H2N-CH2-CH2,
故答案为:CH2=NH+HCN→H2N-CH2-CH2;
(4)甘氨酸的同分异构体的结构简式:CH3CH2NO2 或 HO-CH2CONH2 等,2分子甘氨酸形成一种二肽的结构简式:H2NCH2CONHCH2COOH,
故答案为:CH3CH2NO2 或 HO-CH2CONH2 等;H2NCH2CONHCH2COOH.
点评 本题考查有机物的合成,根据转化故选中分子式判断发生的反应,侧重考查学生分析推理能力,难度不大.

练习册系列答案
相关题目
11.下列离子方程式中正确的是( )
| A. | H2SO4与Ba(OH)2溶液反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| C. | 向Na2CO3溶液中通入少量CO2:CO32-+CO2+H2O═2HCO3- | |
| D. | CH3COOH溶液与NaOH溶液反应:H++OH-═H2O |
9.关于反应方程式Cl2+2I-═2Cl-+I2,说法不正确的是( )
| A. | Cl2是氧化剂 | B. | I2是还原产物 | ||
| C. | 上述反应属于置换反应 | D. | 上述反应属于离子反应 |
16.已知苹果酸的结构简式为: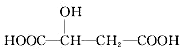 下列说法正确的是( )
下列说法正确的是( )
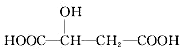 下列说法正确的是( )
下列说法正确的是( )| A. | 苹果酸分子中存在5种不同种类的氢原子 | |
| B. | 1mol苹果酸可与3mol NaOH完全中和 | |
| C. | 苹果酸与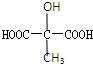 互为同分异构体 互为同分异构体 | |
| D. | 苹果酸分子中的所有碳原子可能处在同一条直线上 |
6.科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空.如图1所示装置中,以稀土金属材料做惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-离子(O2+4e→2O2-).下列说法不正确的是( )


| A. | c电极的名称为正极,d电极上的电极反应式为CH4-8e-+4O2-═CO2+2H2O | |
| B. | 如图2所示,a电极上的电极反应式为4OH--4e-═2H2O+O2↑ | |
| C. | 如图2所示电解100mL0.5mol/LCuSO4溶液,若a电极产生56mL(标准状况)气体,则所得溶液的pH=1(不考虑溶液体积变化) | |
| D. | 若要使电解质溶液恢复到电解前的状态,可加入Cu2(OH)2CO3 |
13.一定条件下,体积为1L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )
| A. | 以X浓度变化表示的反应速率为0.01mol•L-1•S-1 | |
| B. | 将容器体积变为2L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 若增大压强,则物质Y的转化率减小 | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H>0 |
11.将一定量的锌与浓度为18.5mol/L的100mL浓硫酸充分反应后,锌完全溶解,同时生成26.88L标准状况下的气体,反应后测得溶液中氢离子浓度为1.0mol/L,则生成的气体的物质的量之比为( )
| A. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{1}{1}$ | B. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{4}{1}$ | C. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{1}{4}$ | D. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{3}{2}$ |