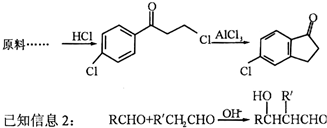
题目内容
6.科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空.如图1所示装置中,以稀土金属材料做惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-离子(O2+4e→2O2-).下列说法不正确的是( )
| A. | c电极的名称为正极,d电极上的电极反应式为CH4-8e-+4O2-═CO2+2H2O | |
| B. | 如图2所示,a电极上的电极反应式为4OH--4e-═2H2O+O2↑ | |
| C. | 如图2所示电解100mL0.5mol/LCuSO4溶液,若a电极产生56mL(标准状况)气体,则所得溶液的pH=1(不考虑溶液体积变化) | |
| D. | 若要使电解质溶液恢复到电解前的状态,可加入Cu2(OH)2CO3 |
分析 依据装置图1中电流流向分析,c为正极,氧气的电子发生还原反应,d为负极,甲烷失电子发生氧化反应;
图2是电解池,与电源正极连接的a电极为阳极,发生4OH--4e-═O2↑+2H2O,b为阴极,发生为Cu2++2e-═Cu,结合电极方程式计算.
解答 解:A.图1是原电池,依据电流流向是从正极流向负极,c电极为正极,d电极为电池负极,d极上甲烷失电子发生还原反应,电极反应为:CH4-8e-+4O2-═CO2+2H2O,故A正确;
B.图2是电解池,与电源正极连接的a电极为阳极,发生4OH--4e-═O2↑+2H2O,故B正确;
C.若a电极产生56mL(标准状况)气体为氧气,物质的量为0.0025mol,消耗氢氧根离子物质的量为0.01mol,溶液中生成氢离子物质的量为0.01mol,c(H+)=$\frac{0.01mol}{0.1L}$=0.1mol/L,pH=-lg0.1=1,故C正确;
D.所得溶液电解过程中CuSO4溶液每损失2个Cu原子,就损失2个 O原子,相当于损失一个CuO,为了使CuSO4溶液,恢复原浓度,应加入CuO,也可以加入CuCO3,符合恢复溶液浓度的定量关系,但不能加入Cu(OH)2、Cu2(OH)2CO3,故D错误.
故选D.
点评 本题考查原电池原理和电解池原理的应用,是中等难度的试题,试题综合性较强,在注重对基础知识巩固和训练的同时,主要是侧重对学生能力的培养,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
16.在短周期元素X、Y、Z,已知X和Y原子核外电子层数相同,Y和Z原子最外层电子数相同.又知三元素最外层电子数之和为14,而质子数之为28.则三种元素有可能是( )
| A. | C、N、P | B. | N、O、S | C. | N、P、F | D. | Be、O、S |
14.下列反应属于消去反应的是( )
| A. | 乙酸与甲醇在浓硫酸作用下共热 | B. | 用丙烯与氯化氢反应制氯丙烷 | ||
| C. | 乙醛与银氨溶液共热 | D. | 溴乙烷与NaOH的醇溶液共热 |
18.关于下图装置,下列说法不正确的是( )
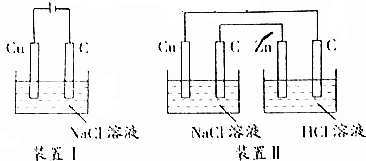

| A. | 装置Ⅰ通电一段时间,可看见溶液变蓝,碳棒上有大量红色物质附着 | |
| B. | 装置Ⅱ能加速铜电极的腐蚀 | |
| C. | 装置Ⅰ将电源换成灵敏电流表,观察到有电流通过 | |
| D. | 装置Ⅰ通电30s后反接电源,再过30s后电极质量未恢复 |
15.浓度均为1mol/L的KCl、CuCl2、AlCl3三种溶液,分别与AgNO3溶液反应,当生成的AgCl沉淀的质量之比为3:2:1时,所用KCl、CuCl2、AlCl3三种溶液的体积比为( )
| A. | 9:6:2 | B. | 9:3:1 | C. | 6:3:2 | D. | 6:3:1 |

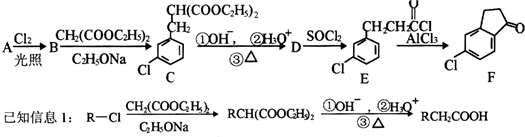
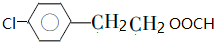 .
. .
.