题目内容
20.(1)25℃时,一定浓度的K2Cr2O7溶液中存在下列平衡:Cr2O72-(橙红色)+H2O?2CrO42-(黄色)+2H+ K=8.3×10-15,则该反应的平衡常数表达式为K=$\frac{{c}^{2}({H}^{+})•{c}^{2}(Cr{O}_{{4}^{2-}})}{c(C{r}_{2}{{O}_{7}}^{2-})}$,取少量上述溶液两等份,分别滴加浓硫酸和浓烧碱溶液,出现的现象依次是显橙红色,显黄色(2)已知在T=298K时,反应:2H2O2(l)═2H2O(l)+O2(g)△H=-196.5kJ/mol
则该正向反应的△S>0,令△G=△H-T△S,判断该正向反应的△G<0,能自发进行(填“能”或“不能”)
研究表明:过氧化氢酶对上述反应的催化效果最佳,这是由于它能极大地降低该反应的活化能.
(3)向K2Cr2O7酸性溶液中加入H2O2,能生成深蓝色的过氧化铬CrO(O2)2 反应如下:Cr2O72-+4H2O2+2H+═2CrO(O2)2+5H2O,类比于Na2O2,判断:该反应不属于(填“属于”或“不属于”)氧化还原反应过氧化铬中铬元素的化合价为+6.
分析 (1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,水不需要写出,据此书写;加入NaOH,中和氢离子,氢离子浓度降低,平衡向右移动;加入酸,H+浓度增大,平衡左移,Cr2O72-浓度增大;
(2)根据产物气体系数和和反应物气体系数和的关系可以判断熵变的符号,根据△G=△H-T△S<0判断反应的自发性;
(3)根据元素的化合价变化情况确定反应是否是氧化还原反应.
解答 解:(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,水不需要写出,即K=$\frac{{c}^{2}({H}^{+})•{c}^{2}(Cr{O}_{{4}^{2-}})}{c(C{r}_{2}{{O}_{7}}^{2-})}$,加入NaOH,中和氢离子,氢离子浓度降低,平衡向右移动,显黄色;加入酸,H+浓度增大,平衡左移,Cr2O72-浓度增大,显橙红色,故答案为:K=$\frac{{c}^{2}({H}^{+})•{c}^{2}(Cr{O}_{{4}^{2-}})}{c(C{r}_{2}{{O}_{7}}^{2-})}$;显橙红色,显黄色;
(2)产物气体系数和大于反应物气体系数和,所以熵变大于零,反应是放热的,得到△G=△H-T△S<0,判断反应是可以自发进行的,过氧化氢酶是催化剂,可以降低反应的活化能,对上述反应的催化效果最佳,故答案为:>;<;能;活化能;
(3)元素的化合价没有变化,确定反应不是氧化还原反应,根据化合价规则,氧化还原反应过氧化铬中铬元素的化合价为+6价,故答案为:不属于;+6.
点评 本题考查学生化学反应速率的计算、化学平衡的移动、反应方向的判断以及氧化还原反应的判断知识,注意知识的迁移应用是关键,难度中等.

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案| A. | Na2CO3溶液(NaHCO3),加入适量的NaOH溶液 | |
| B. | Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液后过滤 | |
| C. | NaHCO3溶液(Na2CO3),通入过量的CO2气体 | |
| D. | Na2O2粉末(Na2O),将混合物在空气中加热 |
| A. | 0.5mo1 C2H4 | B. | 11.2L(标准状况) C2H2 气体 | ||
| C. | 23g Na | D. | 9g H2O |
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小 | |
| D. | 在一定条件下,某可逆反应正向是吸热反应,则其逆向必是放热反应 |
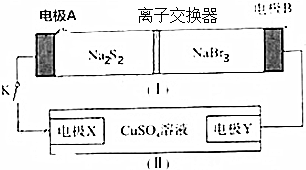
| A. | 装置①中钠离子从右到左通过离子交换膜 | |
| B. | B极的电极反应式为NaBr3+2e-+2Na═3NaBr | |
| C. | X电极的电极反应式为2Cl--2e-═Cl2↑ | |
| D. | 每有0.1mol Na+通过离子交换膜,X电极上析出固体物质0.64g |
| A. | 该反应的△H>0 | |
| B. | 恒温恒容下,增大压强,H2浓度一定减小 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应化学方程式CO+H2O(g)$?_{高温}^{催化剂}$CO2+H2 |
| A. | 20g | B. | 25.4g | C. | 31.6g | D. | 34.8g |
| A. | 该溶液中,K+、Fe2+、I-、Br-可以大量共存 | |
| B. | 和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 | |
| C. | 1L0.1mol/L该溶液和足量的Cu充分反应,离子方程式为Cu+2Fe3+═Cu2++2Fe2+ | |
| D. | 和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
