16.下列分散系能产生丁达尔效应的是( )
| A. | 稀豆浆 | B. | 稀硫酸 | C. | 氢氧化钠溶液 | D. | 食盐水 |
14.下列有关仪器的使用方法或实验操作正确的是( )
| A. | 实验室配制一定物质的量浓度NaCl溶液,用托盘天平秤取5.85gNaCl | |
| B. | 用容量瓶配制溶液时先将容量瓶洗涤并烘干 | |
| C. | 向试管中滴加液体时,胶头滴管紧贴试管内壁 | |
| D. | 酸碱滴定时当指示剂变色后保持半分钟内不变色即达滴定终点 |
12.在通常条件下,NO2和SO2可以很容易发生反应生成NO和SO3.现将碳跟浓硫酸共热产生的气体X和碳跟浓硝酸共热产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )

| A. | 洗气瓶中产生的沉淀是碳酸钡 | |
| B. | 洗气瓶中产生的沉淀是硫酸钡 | |
| C. | 在Z导管出来的气体中无二氧化碳 | |
| D. | 反应一段时间后洗气瓶中溶液的酸性减弱 |
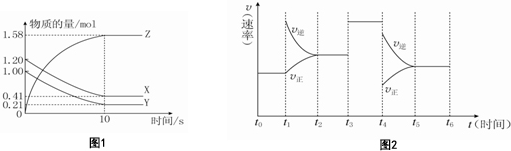
11.对可逆反应4NH3(g)+5O2(g)═4NO(g)+6H2O(g)?下列叙述正确的是( )
| A. | ?达到化学平衡时?4v正(O2)=5v逆(NO) | |
| B. | ?若单位时间内生成x mol NO的同时消耗x mol NH3?则反应达到平衡状态 | |
| C. | ?达到化学平衡时若增大容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | ?当混合气体的压强不随时间变化时,此反应达平衡 |
9. I.下表是A、B、C、D、E五种短周期元素的某些性质:
I.下表是A、B、C、D、E五种短周期元素的某些性质:
(1)E原子的外围电子排布式为2s22p5.
(2)与AD2互为等电子体的分子化学式为N2O(写出一种).
(3)BD2分子中B原子的杂化方式为sp2杂化,分子的立体构型为V形.
Ⅱ.下表是部分金属元素的电离能.
(4)已知X、Y、Z的价层电子构型为ns1,则三种金属的氯化物( RCl)的熔点由低到高的顺序为ZCl<YCl<XCl.
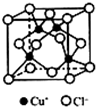
(5)氯化亚铜常用作有机合成催化剂,并用于颜料,防腐等工业.氯化亚铜的晶体结构如图所示.与同一个Cl-相连的Cu+有4个.若晶胞的边长为a cm,则该品体的密度为$\frac{398}{{N}_{A}×{a}^{3}}$g•cm-3.(设NA为阿伏加德罗常数的值)
 I.下表是A、B、C、D、E五种短周期元素的某些性质:
I.下表是A、B、C、D、E五种短周期元素的某些性质:| A | B | C | D | E | |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.5 | 2.5 | 3.0 | 3.5 | 4.0 |
(2)与AD2互为等电子体的分子化学式为N2O(写出一种).
(3)BD2分子中B原子的杂化方式为sp2杂化,分子的立体构型为V形.
Ⅱ.下表是部分金属元素的电离能.
| X | Y | Z | |
| 第一电离能/(kJ/mol) | 520.2 | 495.8 | 418.8 |
(5)氯化亚铜常用作有机合成催化剂,并用于颜料,防腐等工业.氯化亚铜的晶体结构如图所示.与同一个Cl-相连的Cu+有4个.若晶胞的边长为a cm,则该品体的密度为$\frac{398}{{N}_{A}×{a}^{3}}$g•cm-3.(设NA为阿伏加德罗常数的值)
8.关于氧化还原反应的说法正确的是( )
0 153211 153219 153225 153229 153235 153237 153241 153247 153249 153255 153261 153265 153267 153271 153277 153279 153285 153289 153291 153295 153297 153301 153303 153305 153306 153307 153309 153310 153311 153313 153315 153319 153321 153325 153327 153331 153337 153339 153345 153349 153351 153355 153361 153367 153369 153375 153379 153381 153387 153391 153397 153405 203614
| A. | 没有单质参加的化合反应一定是非氧化还原反应 | |
| B. | 金属单质只有还原性,非金属单质只有氧化性 | |
| C. | H2O既有氧化性又有还原性 | |
| D. | KMnO4是一种强氧化剂,没有还原性 |
 硫及其化合物广泛存在于自然界中,回答下列问题:
硫及其化合物广泛存在于自然界中,回答下列问题: