题目内容
13.按要求书写方程式(1)写出氯化铵与氢氧化钠溶液共热的化学方程式NH4Cl+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+H2O+NH3↑
(2)Ba(OH)2的电离方程式Ba(OH)2=Ba2++2OH-
(3)Al2(SO4)3的电离方程式Al2(SO4)3=2Al3++3SO42-.
分析 (1)铵盐和碱反应生成氨气,氯化铵与氢氧化钠溶液共热反应生成氯化钠、氨气、水;
(2)氢氧化钡为强电解质,完全电离成钡离子和氢氧根离子,用等号;
(3)硫酸铝属于盐,为强电解质,完全电离出铝离子和硫酸根离子.
解答 解:(1)氯化铵与氢氧化钠溶液共热反应生成氯化钠、氨气、水,反应的化学方程式为:NH4Cl+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+H2O+NH3↑,
故答案为:NH4Cl+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+H2O+NH3↑;
(2)氢氧化钡为强电解质,完全电离,电离方程式为:Ba(OH)2=Ba2++2OH-,故答案为:Ba(OH)2=Ba2++2OH-;
(3)硫酸铝强电解质,电离时电离出自由移动的铝离子和硫酸根离子,电离方程式为Al2(SO4)3=2Al3++3SO42-,故答案为:Al2(SO4)3=2Al3++3SO42-.
点评 本题主要考查了化学方程式、电离方程式的书写,化学方程式需掌握反应原理,电离方程式的书写,明确电解质的强弱及电离方程式的书写规则是解本题关键,注意原子团不能拆开,题目难度不大.

练习册系列答案
相关题目
12.有X、Y、Z、W四种主族元素,若已知阳离子X、Y和阴离子Z、W具有相同的电子层结构,并且离子径X>Y、Z>W,则四种元素的原子序数为( )
| A. | W>Y>Z>X | B. | Y>X>W>Z | C. | Y>X>Z>W | D. | Z>Y>X>W |
4.除去下列物质中含有的少量杂质(括号中的物质)的方法,错误的是( )
| A. | NH4Cl溶液(I2)用CCl4萃取 | B. | NO(NH3)通过水洗涤 | ||
| C. | NaCl(NH4Cl)加热固体混合物 | D. | N2(NO2)通过水洗涤 |
1.在酸性溶液中,能大量共存的离子组是( )
| A. | Mg2+、Fe3+、NO3-、SCN- | B. | Al3+、Fe2+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、HCO3- | D. | Na+、Ca2+、NO3-、OH- |
8.关于氧化还原反应的说法正确的是( )
| A. | 没有单质参加的化合反应一定是非氧化还原反应 | |
| B. | 金属单质只有还原性,非金属单质只有氧化性 | |
| C. | H2O既有氧化性又有还原性 | |
| D. | KMnO4是一种强氧化剂,没有还原性 |
18. 元素周期表的用途广泛.
元素周期表的用途广泛.
(1)用“>”或“<”填空:
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是bc(填序号).
a.Cl2、Br2、I2的熔点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液$→_{Ⅰ}^{80℃,通电}$NaClO3溶液$→_{Ⅱ}^{室温,KCl}$KClO3晶体
①完成Ⅰ中反应的总化学方程式:□NaCl+□H2O═□NaClO3+□3H2↑.
②Ⅱ中转化的基本反应类型是复分解反应,该反应过程能析出KClO3晶体而无其它晶体析出的原因是室温下KClO3在水中的溶解度明显小于其它晶体.
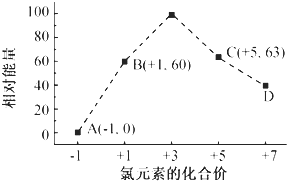
(4)一定条件,在水溶液中1mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示.
①D是ClO4-(填离子符号).
②B→A+C反应的热化学方程式为3ClO-(aq)═(aq)+2Cl-(aq)△H=-117kJ/mol(用离子符号表示)
 元素周期表的用途广泛.
元素周期表的用途广泛.(1)用“>”或“<”填空:
| 离子半径 | 非金属性 | 酸性 | 沸点 |
| K+<S2- | N<O | 硫酸<高氯酸 | HF>HCl |
a.Cl2、Br2、I2的熔点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d.HCl、HBr、HI的酸性
(3)工业上,通过如下转化可制得KClO3晶体:
NaCl溶液$→_{Ⅰ}^{80℃,通电}$NaClO3溶液$→_{Ⅱ}^{室温,KCl}$KClO3晶体
①完成Ⅰ中反应的总化学方程式:□NaCl+□H2O═□NaClO3+□3H2↑.
②Ⅱ中转化的基本反应类型是复分解反应,该反应过程能析出KClO3晶体而无其它晶体析出的原因是室温下KClO3在水中的溶解度明显小于其它晶体.
(4)一定条件,在水溶液中1mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示.
①D是ClO4-(填离子符号).
②B→A+C反应的热化学方程式为3ClO-(aq)═(aq)+2Cl-(aq)△H=-117kJ/mol(用离子符号表示)
5.下列说法中正确的是 ( )

| A. | 氯气通入澄清石灰水中,制取漂白粉 | |
| B. | 可通过化合反应得到Fe(OH)3 | |
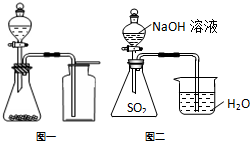
| C. | 选择合适的试剂,用图一所示装置可分别制取少量CO2、NO和O2 | |
| D. | 用图二的装置可证明SO2与NaOH发生了化学反应 |
2.在一密闭容器中,反应aA(g)+bB(g)?mC(s)+nD(g)达到平衡,保持温度不变,将容器体积减小为原来体积的$\frac{1}{2}$,达到新的平衡时,D的浓度是原来的1.7倍,下列说法正确的是( )
| A. | 物质B的转化率增大 | B. | 平衡向正反应方向移动 | ||
| C. | 物质A的体积分数增大 | D. | a+b<m+n |
3.在饱和Ca(OH)2溶液中,加入少量CaO粉末并恢复至原温度后,下列说法正确的是( )
| A. | 溶液中Ca2+的浓度减小 | B. | 溶液质量增大 | ||
| C. | 溶液中Ca(OH)2的质量分数不变 | D. | 溶液中OH-的物质的量不变 |