题目内容
16.下列分散系能产生丁达尔效应的是( )| A. | 稀豆浆 | B. | 稀硫酸 | C. | 氢氧化钠溶液 | D. | 食盐水 |
分析 胶体能产生丁达尔效应,溶液不能产生丁达尔效应,依次分析.
解答 解:A.稀豆浆属于胶体,能产生丁达尔效应,故A正确;
B.稀硫酸属于溶液,不是胶体,不能产生丁达尔效应,故B错误;
C.氢氧化钠溶液属于溶液,不是胶体,不能产生丁达尔效应,故C错误;
D.食盐水属于溶液,不是胶体,不能产生丁达尔效应,故D错误;
故选A.
点评 本题考查了胶体的性质,难度不大,掌握常见的胶体是解题的关键,学习中注意基础知识的积累.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
15.几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X单质、Y单质工业上均用电解其氧化物法得来 | |
| B. | Z、W两元素形成的不同化合物,Z的化合价一定不同 | |
| C. | Y的氧化物能与酸反应也能与碱反应,所以既是酸性氧化物又是碱性氧化物 | |
| D. | 一定条件下,W单质可以将Z单质从其氢化物中置换出来 |
7.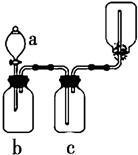 下图装置可用于制取、并收集表格中的四种气体(a、b、c表示相应仪器中加入的试剂)其中可行的是 ( )
下图装置可用于制取、并收集表格中的四种气体(a、b、c表示相应仪器中加入的试剂)其中可行的是 ( )
 下图装置可用于制取、并收集表格中的四种气体(a、b、c表示相应仪器中加入的试剂)其中可行的是 ( )
下图装置可用于制取、并收集表格中的四种气体(a、b、c表示相应仪器中加入的试剂)其中可行的是 ( )| 选项 | 气体 | a | b | c |
| A | NO2 | 浓硝酸 | 铜片 | NaOH溶液 |
| B | SO2 | 浓硫酸 | 铜片 | 酸性KMnO4溶液 |
| C | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
| D | CO2 | 稀盐酸 | 碳酸钙 | 浓硫酸 |
| A. | A | B. | B | ||
| C. | C D.D |
11.对可逆反应4NH3(g)+5O2(g)═4NO(g)+6H2O(g)?下列叙述正确的是( )
| A. | ?达到化学平衡时?4v正(O2)=5v逆(NO) | |
| B. | ?若单位时间内生成x mol NO的同时消耗x mol NH3?则反应达到平衡状态 | |
| C. | ?达到化学平衡时若增大容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | ?当混合气体的压强不随时间变化时,此反应达平衡 |
1.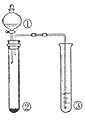 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )
 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 |
| A | 稀硫酸 | Na2S | CuSO4 | 酸性:H2S>H2SO4 |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可以生成白色沉淀 |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
8.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 25℃时,1LpH=12的Ba(OH)2溶液中含有的OH-数目为0.02NA | |
| B. | 室温下,14.0g乙烯和丁烯的混合气体中含有的C-H键数目为2NA | |
| C. | 0.1molFe在0.1molCl2中充分燃烧,转移的电子数为0.3NA | |
| D. | 标准状况下,22.4LCCl4中含有的分子数目为NA |
5.下列有关说法中正确的是( )
| A. | 离子化合物熔沸点较高、共价化合物熔沸点较低 | |
| B. | 全部由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 离子半径:Na+>Mg2+>Al3+>F- | |
| D. | 熔点:金刚石>NaCl>CO2 |
6.如图所示,a、b是两根石墨棒.下列叙述正确的是( )
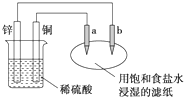

| A. | a为阳极,发生氧化反应:锌为负极被还原 | |
| B. | 电路中电子流动方向:锌→b→a→铜 | |
| C. | 电路中通过0.2mol电子,铜片上产生2.24L气体 | |
| D. | 往滤纸上滴加酚酞,b极附近颜色变红 |
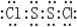 .Y2 Z2遇水很易反应,产生的气体能使品红溶液褪色,则其与水反应的化学方程式为2S2Cl2+2H2O═SO2↑+3S↓+4HCl
.Y2 Z2遇水很易反应,产生的气体能使品红溶液褪色,则其与水反应的化学方程式为2S2Cl2+2H2O═SO2↑+3S↓+4HCl