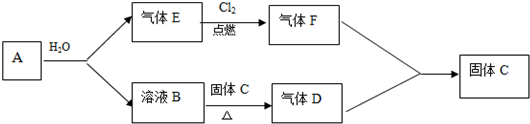
7.下列实验中,依据实验操作及现象,得出的结论不正确的是( )
| 操 作 | 现 象 | 结 论 | |
| A | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| B | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化 但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al |
| C | 无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| D | 向溶液X中加入稀盐酸,并将产生的无色无味气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中可能含有 CO32-或 HCO3- |
| A. | A | B. | B | C. | C | D. | D |
6.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 5.6 g铁与足量盐酸反应转移的电子数为0.3NA | |
| B. | 常温常压下,11.2L二氧化硫中含有的氧原子数为NA | |
| C. | 常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA | |
| D. | 标准状况下,22.4 L氦气与22.4 L氮气所含原子数均为2 NA |
5.在120℃时,在一密闭容器中有CO、H2、O2混合气体共28.5g,用电火花引燃,使其完全燃烧,再将燃烧后的气体用过量的Na2O2充分吸收,固体增重12.5g,则原混合气体中O2的物质的量是( )
| A. | 0.35mol | B. | 0.45 mol | C. | 0.50 mol | D. | 1.00mol |
4.下列离子方程式书写正确的是( )
| A. | 铁与稀硫酸反应 Fe+2H+═Fe3++H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 碳酸钡与盐酸反应 CO32-+2H+═H2O+CO2↑ | |
| D. | 氢氧化钠溶液与硫酸铜溶液反应 2OH-+Cu2+═Cu(OH)2↓ |
3.除去KCl(aq)中混有的少量MgSO4(aq表示溶液),所选用的一种适量的试剂是( )
| A. | KOH(aq) | B. | NaOH(aq) | C. | BaCl2(aq) | D. | Ba(OH)2(aq) |
2.下列说法正确的是( )
| A. | 某溶液中滴入AgNO3溶液,生成白色沉淀,该溶液中可能含Cl- | |
| B. | 实验已经证明,氯水是可以导电的,所以氯水是电解质 | |
| C. | 某溶液与淀粉碘化钾溶液反应后出现蓝色,则证明该溶液是氯水 | |
| D. | 胶体与其它分散系的本质区别在于胶体具有丁达尔效应 |
1.化学知识在生活中有重要意义,下列说法不正确的是( )
| A. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| B. | 小苏打用于治疗胃溃疡病人的胃酸过多症 | |
| C. | 计算机芯片所用的材料是高纯度的硅 | |
| D. | 纯净的二氧化硅是生产光纤制品的基本原料 |
20.将3.9g镁铝合金,投入到500mL 2mol/L的盐酸中,金属完全溶解,再加入4mol/L的NaOH溶液,若要生成的沉淀最多,加入的这种NaOH溶液的体积是( )
0 152724 152732 152738 152742 152748 152750 152754 152760 152762 152768 152774 152778 152780 152784 152790 152792 152798 152802 152804 152808 152810 152814 152816 152818 152819 152820 152822 152823 152824 152826 152828 152832 152834 152838 152840 152844 152850 152852 152858 152862 152864 152868 152874 152880 152882 152888 152892 152894 152900 152904 152910 152918 203614
| A. | 125 mL | B. | 200 mL | C. | 250 mL | D. | 560 mL |