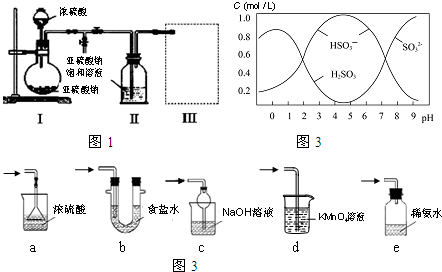
9.下列实验现象的描述错误的是( )
| A. | 氢气在氯气中燃烧生成黄绿色烟雾 | |
| B. | 红热的铁丝在氧气中燃烧,火星四射,生成黑色固体颗粒 | |
| C. | 点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰 | |
| D. | 钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体 |
5. 海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.
海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.
(1)氯原子结构示意图是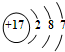 ,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).
,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).
(2)向浓缩的海水中通入Cl2,可将Br-转化为Br2.再用“空气吹出法”将Br2从浓海水中吹出,并用纯碱浓溶液吸收,生成NaBr、NaBrO3等.当有1mol Br2被纯碱吸收时,转移的电子数为1×1024.
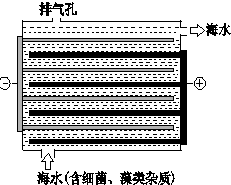
(3)如图是NaClO的发生装置.该装置主要利用了电解饱和食盐水的原理,可实现对海水的消毒和灭藻.
①写出装置中产生NaClO的化学方程式2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,2NaOH+Cl2→NaClO+NaCl+H2O.
海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH)2和CaCO3.生成CaCO3的离子方程式是Ca2++HCO3-+OH-→CaCO3↓+H2O.
若每隔5-10min倒换一次电极电性,可有效地解决阴极的结垢问题.试用电极反应式并结合必要的文字进行解释阴极结垢后倒换电极电性,阴极变为阳极,其电极反应为:2Cl--2e→Cl2↑,产生的氯气与水发生反应:Cl2+H2=HCl+HClO,使该电极附近溶液呈酸性,从而将Mg(OH)2和CaCO3溶解而达到除垢的目的.
NaOH溶液吸收SO2得Na2SO3,可用Na2SO3吸收SO2.在SO2被吸收的过程中,pH随n(SO32-)、n(HSO3-)变化关系如下:
②从上表可判断,NaHSO3溶液呈酸性(填“酸性”、“碱性”、“中性”),请用平衡原理解释:HSO3-存在HSO3-?H++SO32-和HSO3-+H2O?H2SO3+OH-,HSO3-的电离程度大于水解程度.
③当吸收液呈中性时,溶液中离子浓度关系正确的是ab(选填字母).
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
d.c(Na+)>c(SO32-)>c(HSO3-)>c(H+)=c(OH-)
 海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.
海洋化学资源的研究和合理利用具有广阔前景,从海水中可提取氯、溴、碘等卤族元素.(1)氯原子结构示意图是
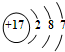 ,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).
,碘在元素周期表中的位置是第五周期ⅦA族,HI的稳定性比HBr弱(填写“强”或“弱”).(2)向浓缩的海水中通入Cl2,可将Br-转化为Br2.再用“空气吹出法”将Br2从浓海水中吹出,并用纯碱浓溶液吸收,生成NaBr、NaBrO3等.当有1mol Br2被纯碱吸收时,转移的电子数为1×1024.
(3)如图是NaClO的发生装置.该装置主要利用了电解饱和食盐水的原理,可实现对海水的消毒和灭藻.
①写出装置中产生NaClO的化学方程式2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,2NaOH+Cl2→NaClO+NaCl+H2O.
海水中含有Ca2+、Mg2+、HCO3-等杂质离子,处理过程中装置的阴极易产生水垢,其主要成分是Mg(OH)2和CaCO3.生成CaCO3的离子方程式是Ca2++HCO3-+OH-→CaCO3↓+H2O.
若每隔5-10min倒换一次电极电性,可有效地解决阴极的结垢问题.试用电极反应式并结合必要的文字进行解释阴极结垢后倒换电极电性,阴极变为阳极,其电极反应为:2Cl--2e→Cl2↑,产生的氯气与水发生反应:Cl2+H2=HCl+HClO,使该电极附近溶液呈酸性,从而将Mg(OH)2和CaCO3溶解而达到除垢的目的.
NaOH溶液吸收SO2得Na2SO3,可用Na2SO3吸收SO2.在SO2被吸收的过程中,pH随n(SO32-)、n(HSO3-)变化关系如下:
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
③当吸收液呈中性时,溶液中离子浓度关系正确的是ab(选填字母).
a.c(Na+)=2c(SO32-)+c(HSO3-)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
d.c(Na+)>c(SO32-)>c(HSO3-)>c(H+)=c(OH-)
3.科学家曾预言一种可用作炸药的物质,分子式为C(N3)4,其爆炸反应方程式为:C(N3)4→C+6N2↑,下列说法一定错误的是( )
| A. | 该物质为离子晶体 | |
| B. | 该物质可用通过C60吸附N2而制得 | |
| C. | C(N3)4中碳元素为正价 | |
| D. | 18g该物质完全分解可以产生13.44升(标准状况)氮气 |
2.25℃时,某溶液中由水电离的氢离子为1×10-12mol/L,关于该溶液的说法正确的是( )
| A. | HCO3-一定不能大量存在 | B. | pH一定是12 | ||
| C. | 加入铝片一定能产生氢气 | D. | 一定不是NH4Cl溶液 |
1.氮化钠和氢化钙都是离子化合物,与水反应的化学方程式(末配平)如下:Na3N+H2O→NaOH+NH3,CaH2+H2O→Ca(OH)2+H2.有关它们的叙述正确的是( )
| A. | 离子半径的大小:Na+>N3->H- | |
| B. | 它们与水发生的反应均属于氧化还原反应 | |
| C. | 两种化合物均只含离子键,不含共价键 | |
| D. | 两固体混合物溶于足量盐酸中可得到三种盐 |
20.某气体的摩尔质量为M g/mol,NA表示阿伏加德罗常数,在一定的温度和压强下,体积为V L的该气体所含有的分子数为X.则$\frac{MX}{V{N}_{A}}$表示的是( )
0 152712 152720 152726 152730 152736 152738 152742 152748 152750 152756 152762 152766 152768 152772 152778 152780 152786 152790 152792 152796 152798 152802 152804 152806 152807 152808 152810 152811 152812 152814 152816 152820 152822 152826 152828 152832 152838 152840 152846 152850 152852 152856 152862 152868 152870 152876 152880 152882 152888 152892 152898 152906 203614
| A. | V L该气体的质量(以g为单位) | B. | 1 L该气体的质量(以g为单位) | ||
| C. | 1 mol该气体的体积(以L为单位) | D. | 1 L该气体的物质的量(以mol为单位) |
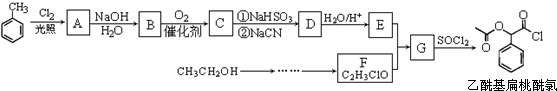
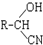 ,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′
,RCN$\stackrel{H_{2}O/H+}{→}$RCOOH,RCOOH$\stackrel{SOCl_{2}}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′ ,E中含氧官能团的名称醇羟基和羧基.
,E中含氧官能团的名称醇羟基和羧基.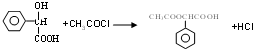 .
.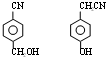 .
.