18.下列叙述正确的是( )
| A. | 同温同压下,相同体积的物质,它们的物质的量一定相等 | |
| B. | 任何条件下,等物质的量的二氧化硫和一氧化碳所含的分子数一定相等 | |
| C. | 1L一氧化碳气体一定比1L氧气的质量小 | |
| D. | 等体积、等物质的量浓度的强酸中所含的H+数一定相等 |
17.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
| A. | H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有氧化性,都是氧化性酸 | |
| C. | HF、HClO、NH3都易溶于水,都是电解质 | |
| D. | C2H2、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
16.下列溶液氯离子的物质的量浓度与50mL 1mol•L-1AlCl3溶液中氯离子的物质的量浓度相等的是( )
| A. | 150 mL 3 mol•L-1氯酸钾溶液 | B. | 75 mL 3 mol•L-1氯化钙溶液 | ||
| C. | 150 mL 3 mol•L-1氯化钾溶液 | D. | 50 mL 3 mol•L-1氯化镁溶液 |
15.若NA表示阿伏加德罗常数,下列关于0.3mol/L的MgCI2溶液的说法正确的是( )
| A. | 100毫升的溶液中含有Mg2+、CI-总数为0.3 NA | |
| B. | 100毫升的溶液中含有Mg2+数目是O.1NA | |
| C. | 2升溶液中Mg2+的浓度是0.3mol/L | |
| D. | 1.5升溶液中含有CI-的浓度是4.5mol/L |
14.能用H++OH-=H2O表示的是( )
0 152676 152684 152690 152694 152700 152702 152706 152712 152714 152720 152726 152730 152732 152736 152742 152744 152750 152754 152756 152760 152762 152766 152768 152770 152771 152772 152774 152775 152776 152778 152780 152784 152786 152790 152792 152796 152802 152804 152810 152814 152816 152820 152826 152832 152834 152840 152844 152846 152852 152856 152862 152870 203614
| A. | NaOH溶液和CO2的反应 | B. | Cu(OH)2和稀H2S04的反应 | ||
| C. | Ba(OH)2溶液和盐酸反应 | D. | CaC03和稀H2S04的反应 |
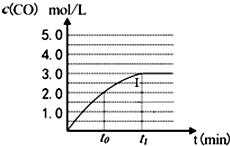 工业上一般在密闭容器中采用下列反应合成甲醇:
工业上一般在密闭容器中采用下列反应合成甲醇:
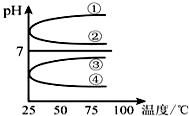 (1)稀释0.1mol•L-1氨水时,随着水量的增加而减小的是①②(填写序号).
(1)稀释0.1mol•L-1氨水时,随着水量的增加而减小的是①②(填写序号).