14.下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A. | NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):c(Na+)=c(HRO3-)+2c(RO32-) | |
| B. | 常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH) | |
| C. | 常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):①<③<② | |
| D. | 等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数多少:N前>N后 |
11.在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加人a mol及b mol碘化氢(a>b),待反应2HI(g)═I2(g)+H2(g)达平衡后,下列说法正确的是( )
| A. | 从反应开始到建立平衡所需时间:tA>tB | |
| B. | 平衡时I2的浓度:c(I2)A=c(I2)B | |
| C. | 平衡时碘蒸气在混合气体中的百分含量:A容器大于B容器 | |
| D. | 平衡时HI的分解率:aA=aB |
9.下列叙述正确的是( )
| A. | 离子晶体中,只存在离子键,不可能存在其它化学键 | |
| B. | 氧族元素(O、S、Se、Te)的氢化物的沸点依次升高 | |
| C. | NaHSO4、Na2O2晶体中的阴阳离子个数比均为1:1 | |
| D. | 晶体的硬度:金刚石>碳化硅>石英 |
8.化学与人类生产、生活、环境保护及社会可持续发展密切相关,下列有关叙述正确的是( )
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | PM2.5表面积大,能吸附大量的有毒有害物质,对人的肺功能造成很大危害 | |
| C. | 二氧化硅广泛应用于太阳能电池、计算机芯片 | |
| D. | 汽车尾气中含有大量大气污染物,这是汽油不完全燃烧造成的 |
7.在酸性Fe(NO3)3溶液中逐渐通入H2S气体,不可能发生的离子反应是( )
| A. | 3H2S+2NO3-+2H+═2NO↑+3S↓+4H2O | |
| B. | 3Fe3++3NO3-+6H2S═3NO↑+6S↓+3Fe2++6H2O | |
| C. | Fe3++3NO3-+5H2S+2H+═3NO↑+5S↓+Fe2++6H2O | |
| D. | Fe3++9NO3-+14H2S+8H+═9NO↑+14S↓+Fe2++18H2O |
6.某离子反应涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中c(NH4+)随反应进行逐渐减小.下列判断正确的是( )
0 152519 152527 152533 152537 152543 152545 152549 152555 152557 152563 152569 152573 152575 152579 152585 152587 152593 152597 152599 152603 152605 152609 152611 152613 152614 152615 152617 152618 152619 152621 152623 152627 152629 152633 152635 152639 152645 152647 152653 152657 152659 152663 152669 152675 152677 152683 152687 152689 152695 152699 152705 152713 203614
| A. | 反应的还原产物是N2 | |
| B. | 消耗1 mol氧化剂,转移电子3 mol | |
| C. | 氧化剂与还原剂的物质的量之比为2:3 | |
| D. | 反应后溶液的酸性明显增强 |
 .
.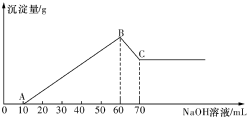 有一澄清透明的溶液,可能大量存在有NH4+、Fe3+、H+、Mg2+、A13+、I-、CO32-等离子.现分别取溶液进行下列实验:
有一澄清透明的溶液,可能大量存在有NH4+、Fe3+、H+、Mg2+、A13+、I-、CO32-等离子.现分别取溶液进行下列实验: ②
② ③
③ ④TNT
④TNT