题目内容
15.用KMnO4氧化溶质质量分数为36.5%的盐酸.反应方程式如下:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O(1)若此盐酸的密度为1.2g/cm3,其物质的量浓度为12mol/L.
(2)用双线桥法表示电子的转移情况
 .
.(3)此反应中氧化剂与还原剂的物质的量的比为1:5.
(4)15.8g KMnO4完全反应,产生标准状况下Cl2的体积为5.6L,反应中转移电子的数目为0.5NA.(用NA表示阿伏加德罗常数的值)
分析 (1)盐酸的物质的量浓度=$\frac{10{\;}^{3}ρω}{M}$;
(2)反应中高锰酸钾为氧化剂,浓盐酸为还原剂,根据Mn元素的化合价+7→+2,和Cl元素的化合价-1→0,标出电子的转移方向和数目;
(3)KMnO4为氧化剂,HCl为还原剂,结合化合价的变化或方程式计算;
(4)根据方程式知,参加反应的HCl有$\frac{5}{8}$被氧化,结合化合价的变化计算.
解答 解:(1)盐酸的物质的量浓度=$\frac{10{\;}^{3}ρω}{M}$=$\frac{10{\;}^{3}×1.2×36.5%}{36.5}$mol/L=12mol/L,故答案为:12mol/L;
(2)反应中高锰酸钾为氧化剂,浓盐酸为还原剂,Mn元素的化合价+7→+2,和Cl元素的化合价-1→0,反应中氧化剂和还原剂得失电子数目相等,可表示为 ,
,
故答案为: ;
;
(3)KMnO4为氧化剂,HCl为还原剂,由2KMnO4~10HCl可知氧化剂与还原剂的物质的量之比为2:10=1:5,故答案为:1:5;
(4)高锰酸钾的量、氯气的量以及消耗的盐酸之间的关系为:2KMnO4~5Cl2~16HCl,被氧化的盐酸和参加反应的盐酸的量之比为:$\frac{5}{8}$,15.8g (即0.1mol)KMnO4完全反应时,产生的Cl2为0.25mol,转移电子0.5mol,数目为0.5NA,在标准状况下的体积为0.25mol×22.4L/mol=5.6L,
故答案为:5.6L;0.5NA;
点评 本题考查氧化还原反应的计算,明确方程式中各个物理量之间的关系式是解本题关键,侧重考查计算能力,注意参加反应的HCl有一部分被氧化,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
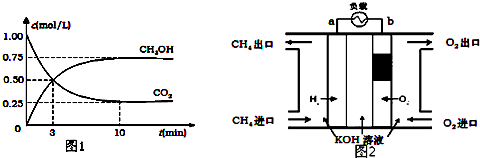
3.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ/mol
则下列说法不正确的是( )
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ/mol
则下列说法不正确的是( )
| A. | CH3OH的燃烧热为192.9 kJ/mol | |
| B. | CH3OH转变成H2的过程不一定要吸收能量 | |
| C. | 根据①②推知反应:H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=+241.9 kJ/mol | |
| D. | 根据②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)的△H>-192.9 kJ/mol |
7.下列变化不能通过一步反应直接完成的是( )
| A. | Al→[Al(OH)4]- | B. | Na2CO3→NaOH | C. | Al2O3→Al(OH)3 | D. | Fe(OH)2→Fe(OH)3 |
4.对于反应 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,以下叙述正确的是( )
| A. | 氧化剂和还原剂的物质的量比为8:3 | |
| B. | 被还原的HNO3和起酸性作用的HNO3的物质的量的比为2:3 | |
| C. | 生成1molNO气体转移的电子数为3NA | |
| D. | 该反应中Cu(NO3)2 为氧化产物,H2O为还原产物 |
9.下列事实不能用元素周期律解释的是( )
| A. | 热稳定性:Na2CO3>NaHCO3 | B. | 酸性:H2CO3>H2SiO3 | ||
| C. | 碱性:NaOH>LiOH | D. | 热稳定性:HF>HBr |
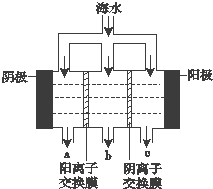 《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.
《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.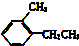 ②
② ③
③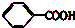 ④TNT
④TNT