4.E和F加入密闭容器中,在一定条件下发生反应:E(s)+4F(g)?G(g),已知该反应的平衡常数值如下表所示.下列说法正确的是( )
| 温度℃ | 25 | 80 | 230 |
| 平衡常数值 | 5×104 | 2 | 1.9×10-5 |
| A. | 上述反应是熵增反应 | |
| B. | 25℃时,反应G(g)?E(s)+4F(g)的平衡常数值是0.5 | |
| C. | 在80℃时,测得某时刻,F、G浓度均为0.5 mol•L-1,则此时v(正)>v(逆) | |
| D. | 恒温恒容下,向容器中再充入少量G(g),达新平衡时,G的体积百分含量将增大 |
20.消除氮氧化物污染有多种方法.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4 (g)+4NO2 (g)═4NO(g)+CO2(g)+2H2 O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)═2N2 (g)+CO2(g)+2H2 O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(1),△H=-955 kJ•mol-1.
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
①不能作为判断反应达到化学平衡状态的依据是B C
A.容器内CO2的浓度保持不变 B.v正(N2)=2v正(NO) C.容器内压强保持不变 D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②计算该温度下该反应的平衡常数为0.56(保留两位小数);
③在30min,改变某一条件,反应重新达到平衡,则改变的条件是减小CO2浓度.
(3)甲烷燃料电池可以提升能量利用率,如图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:
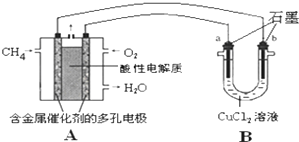
请回答:
①甲烷燃料电池的负极反应式是CH4-8e─+2H2O=CO2+8H+
②当A中消耗0.15mol氧气时,B中b(用a或b 表示)极增重19.2g.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4 (g)+4NO2 (g)═4NO(g)+CO2(g)+2H2 O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)═2N2 (g)+CO2(g)+2H2 O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(1),△H=-955 kJ•mol-1.
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
A.容器内CO2的浓度保持不变 B.v正(N2)=2v正(NO) C.容器内压强保持不变 D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②计算该温度下该反应的平衡常数为0.56(保留两位小数);
③在30min,改变某一条件,反应重新达到平衡,则改变的条件是减小CO2浓度.
(3)甲烷燃料电池可以提升能量利用率,如图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:

请回答:
①甲烷燃料电池的负极反应式是CH4-8e─+2H2O=CO2+8H+
②当A中消耗0.15mol氧气时,B中b(用a或b 表示)极增重19.2g.
19. 硫及其化合物对人类的生产和生活有着重要的作用.
硫及其化合物对人类的生产和生活有着重要的作用.
2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1是制备硫酸的重要反应.
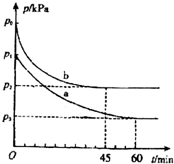
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2,反应在不同条件下进行,反应体系总压强随时间的变化如下图所示.与实验a相比,实验b改变的条件是升高温度,判断的依据实验b与a相比,反应速率快,平衡向逆反应方向移动.
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)?SO3(g)+NO(g)△H=-42kJ•mol-1.
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)=0.05mol/(L.min),该温度下的平衡常数2.613.
②实验丙中,达到平衡时,NO2的转化率为$\frac{10a}{3}$×100%.
③由表中数据可推知,Tl<T2(填“>”“<’’或“=”),判断的理由是T1时,该反应的平衡常数K1=2.613,T2时,该反应的平衡常数K2=1,该反应正反应为放热反应,所以T1<T2.
 硫及其化合物对人类的生产和生活有着重要的作用.
硫及其化合物对人类的生产和生活有着重要的作用.2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1是制备硫酸的重要反应.
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2,反应在不同条件下进行,反应体系总压强随时间的变化如下图所示.与实验a相比,实验b改变的条件是升高温度,判断的依据实验b与a相比,反应速率快,平衡向逆反应方向移动.
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)?SO3(g)+NO(g)△H=-42kJ•mol-1.
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
| 实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
| N(SO2) | N(NO2) | N(NO) | ||
| 甲 | T1 | 0.80 | 0.20 | 0.18 |
| 乙 | T2 | 0.20 | 0.80 | 0.16 |
| 丙 | T3 | 0.20 | 0.30 | a |
②实验丙中,达到平衡时,NO2的转化率为$\frac{10a}{3}$×100%.
③由表中数据可推知,Tl<T2(填“>”“<’’或“=”),判断的理由是T1时,该反应的平衡常数K1=2.613,T2时,该反应的平衡常数K2=1,该反应正反应为放热反应,所以T1<T2.
18.T℃时,在容积为2L的3个恒容密闭容器中发生反应:3A(g)+B(g)?xC(g),按不同方式投入反应物,测得反应达到平衡时的有关数据如下:
下列说法正确的是( )
0 152413 152421 152427 152431 152437 152439 152443 152449 152451 152457 152463 152467 152469 152473 152479 152481 152487 152491 152493 152497 152499 152503 152505 152507 152508 152509 152511 152512 152513 152515 152517 152521 152523 152527 152529 152533 152539 152541 152547 152551 152553 152557 152563 152569 152571 152577 152581 152583 152589 152593 152599 152607 203614
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3mol A、2mol B | 6mol A、4mol B | 2mol C |
| 到达平衡的时间(min) | 5 | 8 | |
| A的浓度(mol/L) | c1 | c2 | |
| C的体积分数 | w1 | w3 | |
| 混合气体密度(g/L) | ρ1 | ρ2 |
| A. | 若x<4,则2c1>c2 | |
| B. | 若x=4,则w3=w1 | |
| C. | 无论x的值是多少,均有2ρ1=ρ2 | |
| D. | 容器甲达到平衡所需的时间比容器乙达到平衡所需的时间短 |