6.下列有关判断的依据正确的是( )
| A. | 电解质:水溶液是否导电 | |
| B. | 原子晶体:构成晶体的微粒是否是原子 | |
| C. | 共价分子:分子中原子间是否全部是共价键 | |
| D. | 化学平衡状态:平衡体系中各组分的物质的量浓度是否相等 |
5.下列有关物质结构的叙述正确的是( )
| A. | 在离子化合物中不可能存在非极性共价键 | |
| B. | 由电子定向移动而导电的物质一定是金属晶体 | |
| C. | 有键能很大的共价键存在的物质熔沸点一定很高 | |
| D. | 只含有共价键的物质不一定是共价化合物 |
3.在标准状况下进行甲、乙、丙三组实验,三组实验均各取30mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据如表:
(1)乙组实验中,盐酸过量(填“过量”、“适量”、“不足量”).
(2)要计算出盐酸的物质的量浓度,题中可作为计算依据的数据是乙或丙,求得盐酸的物质的量浓度为1mol/L.
(3)求合金中镁、铝的物质的量之比,题中可作为计算依据的数据是甲,求得的镁、铝的物质的量之比是1:1.
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(2)要计算出盐酸的物质的量浓度,题中可作为计算依据的数据是乙或丙,求得盐酸的物质的量浓度为1mol/L.
(3)求合金中镁、铝的物质的量之比,题中可作为计算依据的数据是甲,求得的镁、铝的物质的量之比是1:1.
19.如表实验能达到预期目的是( )
| 实验内容 | 实验目的 | |
| A | 向新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液先变红色后褪色 | 证明有氯水具有酸性 |
| B | 将Cl2通入NaBr溶液中,溶液变黄 | 比较氯气比液溴的氧化性强 |
| C | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 证明氧化性:Cu2+>Fe3+ |
| D | 向某待测溶液中,加入BaCl2溶液,产生白色沉淀,继续滴加稀盐酸,沉淀不消失 | 证明待测溶液中含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
18.下列叙述正确的是( )
(1)二氧化硫使品红溶液,溴水和酸性高锰酸钾溶液褪色是因为二氧化硫具有漂白性.
(2)二氧化硫溶于水得到的溶液有氧化性,还原性,酸性.
(3)二氧化硫通入氢氧化钡溶液中,有白色沉淀生成,加入盐酸沉淀溶解.
(4)二氧化硫通入氯化钡溶液中有沉淀生成.
(1)二氧化硫使品红溶液,溴水和酸性高锰酸钾溶液褪色是因为二氧化硫具有漂白性.
(2)二氧化硫溶于水得到的溶液有氧化性,还原性,酸性.
(3)二氧化硫通入氢氧化钡溶液中,有白色沉淀生成,加入盐酸沉淀溶解.
(4)二氧化硫通入氯化钡溶液中有沉淀生成.
| A. | (1)(4) | B. | (4)(3) | C. | (1)(2) | D. | (2)(3) |
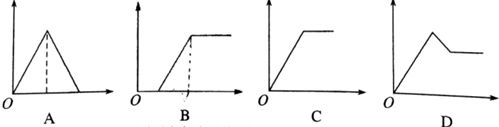
17. 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.往溶液滴加NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.往溶液滴加NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )
0 152331 152339 152345 152349 152355 152357 152361 152367 152369 152375 152381 152385 152387 152391 152397 152399 152405 152409 152411 152415 152417 152421 152423 152425 152426 152427 152429 152430 152431 152433 152435 152439 152441 152445 152447 152451 152457 152459 152465 152469 152471 152475 152481 152487 152489 152495 152499 152501 152507 152511 152517 152525 203614
 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.往溶液滴加NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.往溶液滴加NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )| A. | 溶液中的阳离子只有H+、NH4+、Mg2+、Al3+ | |
| B. | 溶液中n(NH4+)=0.2mol | |
| C. | 溶液中一定不含CO32-,可能含有SO42-和NO3- | |
| D. | n(H+):n(Al3+):n(Mg2+)=1:1:1 |
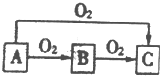 A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物)
A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物)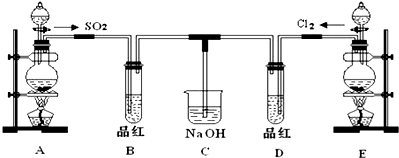
 ;请指出该反应中的液体反应物在反应中所表现出的化学性质:还原性和酸性;若液体中的溶质反应了6mol,则转移的电子的物质的量3mol;
;请指出该反应中的液体反应物在反应中所表现出的化学性质:还原性和酸性;若液体中的溶质反应了6mol,则转移的电子的物质的量3mol;