题目内容
18.下列叙述正确的是( )(1)二氧化硫使品红溶液,溴水和酸性高锰酸钾溶液褪色是因为二氧化硫具有漂白性.
(2)二氧化硫溶于水得到的溶液有氧化性,还原性,酸性.
(3)二氧化硫通入氢氧化钡溶液中,有白色沉淀生成,加入盐酸沉淀溶解.
(4)二氧化硫通入氯化钡溶液中有沉淀生成.
| A. | (1)(4) | B. | (4)(3) | C. | (1)(2) | D. | (2)(3) |
分析 二氧化硫为酸性氧化物,能够与碱反应生成盐和水,具有漂白性、还原性和弱的氧化性,据此解答.
解答 解:(1)二氧化硫具有漂白性,能够使品红褪色,具有还原性,能够还原溴水和酸性高锰酸钾溶液使其褪色,故错误;
(2)二氧化硫与水反应生成亚硫酸,亚硫酸具有酸性,亚硫酸中硫为+4价,处于中间价态,既有氧化性又具有还原性,故正确;
(3)二氧化硫与氢氧化钡反应生成亚硫酸钡沉淀和水,亚硫酸钡与盐酸反应生成氯化钡和二氧化硫、水,故正确;
(4)亚硫酸酸性弱于盐酸,二氧化硫与氯化钡溶液不反应,故错误;
故选:D.
点评 本题考查了二氧化硫的性质,熟悉二氧化硫的漂白性、还原性、酸性氧化物的性质即可解答,题目难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
9.下列反应的离子方程式正确的是( )
| A. | 铁与硫酸铜溶液反应:Fe+Cu2+═Cu+Fe 3+ | |
| B. | 铜与稀硝酸反应:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
6.针对下面10种元素,完成以下各小题.回答下列间题.
(1)非金属性最强的元素是氟(填名称).化学性质最不活泼的元素是Ne(填元素符号).
(2)S 原子结构示意图为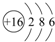 ;
;
(3)Mg和Al中,原子半径较小的是Al;
(4)N的氢化物的分子式NH3,该物质中N元素与H元素的质量比为14:3,(相对原子质量:N-14 H-1),其水溶液呈碱性性.
(5)元素硅的氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(6)元素最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式),呈两性的是Al(OH)3(填化学式);两者反应的化学方程式NaOH+Al(OH)3=NaAlO2+2H2O.
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | C | N | F | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)S 原子结构示意图为
 ;
;(3)Mg和Al中,原子半径较小的是Al;
(4)N的氢化物的分子式NH3,该物质中N元素与H元素的质量比为14:3,(相对原子质量:N-14 H-1),其水溶液呈碱性性.
(5)元素硅的氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称);
(6)元素最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式),呈两性的是Al(OH)3(填化学式);两者反应的化学方程式NaOH+Al(OH)3=NaAlO2+2H2O.
13.2015年初,全国范围内遭遇了严重的雾霾天气,为了改善空气质量,政府提出减少化石能源的使用,提倡新能源,国家大力扶持光电产业,下列说法错误的是( )
| A. | 光伏发电主要利用高纯度单质硅制成的硅太阳能电池 | |
| B. | 硅太阳能电池可将太阳能直接转化为电能,减少化石燃料的使用,保护环境 | |
| C. | 硅的结构和金刚石类似,是具有金属光泽的灰黑色固体 | |
| D. | 硅单质即能与氢氧化钠反应又能与氢氟酸反应,所以硅是两性 |
3.在标准状况下进行甲、乙、丙三组实验,三组实验均各取30mL同浓度的盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据如表:
(1)乙组实验中,盐酸过量(填“过量”、“适量”、“不足量”).
(2)要计算出盐酸的物质的量浓度,题中可作为计算依据的数据是乙或丙,求得盐酸的物质的量浓度为1mol/L.
(3)求合金中镁、铝的物质的量之比,题中可作为计算依据的数据是甲,求得的镁、铝的物质的量之比是1:1.
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(2)要计算出盐酸的物质的量浓度,题中可作为计算依据的数据是乙或丙,求得盐酸的物质的量浓度为1mol/L.
(3)求合金中镁、铝的物质的量之比,题中可作为计算依据的数据是甲,求得的镁、铝的物质的量之比是1:1.
10.PbO2在酸性溶液中能将Mn2+氧化成MnO4-,本身被还原为Pb2+.取一支试管,加入适量PbO2固体和适量的稀H2SO4后滴入2mL 1mol/L MnSO4溶液.下列说法错误的是( )
| A. | 上述实验中不能用盐酸代替硫酸 | |
| B. | 将试管充分振荡后静置,溶液颜色变为紫色 | |
| C. | 在酸性条件下,PbO2的氧化性比MnO4-的氧化性强 | |
| D. | 若硫酸锰充分反应,消耗PbO2的物质的量为0.01mol |
7.R分子的质量为a g,相对质量为M,则M与a的比值等于( )
| A. | 6.02×1023 | B. | 12C原子质量的十二分之一 | ||
| C. | 0.012Kg12C所含的原子数 | D. | 1mol氧气所含的微粒数 |
8.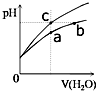 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )
 某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是( )| A. | a、b、c三点溶液的离子浓度之和a>b>c | |
| B. | b点溶液中c(H+)+c(NH3•H2O)=c(OH-) | |
| C. | 用等浓度的NaOH溶液和等体积b、c处溶液反应,恰好反应时消耗NaOH溶液的体积Vb=Vc | |
| D. | a、b、c三点溶液中水的电离程度a>b>c |