10.在强酸性溶液中,可以大量共存的离子组是( )
| A. | Na+、K+、S2-、Cl- | B. | Al3+、Mg2+、SO42-、Cl- | ||
| C. | K+、Na+、SiO32-、NO3- | D. | K+、Na+、SO42-、CO32- |
8.将0.3mol KCl、0.2mol Cu(N03)2、0.1mol AgN03一起溶于水,配成100mL混合溶液,用惰性电极电解一段时间后,若在一极析出9.6g Cu,此时在另一极上产生的气体体积(标准状况)为( )
| A. | 2.24L | B. | 3.92L | C. | 3.36L | D. | 2.8L |
7.向含有90g Nal溶液中加入40g溴单质后,再向溶液中通入过量的氯气,完全反应后.被还原的氯气的质量为( )
| A. | 42.0g | B. | 21.3g | C. | 7.1g | D. | 3.55g |
6.常温下,氮的氧化物(NOx)中除五氧化二氮为固体外,其余均为气体.五氧化二氮的熔点为30℃,则等质量的N2O、N0、N2O5三种物质在常温下体积的大小顺序是( )
| A. | N2O>NO>N2O5 | B. | NO>N2O>N2O5 | C. | N2O5>NO>N2O | D. | N2O5>N2O>NO |
4.下列说法正确的是( )
| A. | 常温常压下,22.4L氮气所含原子数目大于2NA | |
| B. | 1 mol Na2O2跟H2O反应转移的电子数目为2NA | |
| C. | 标准状态下,22.4L三氧化硫所含分子数目大于NA | |
| D. | 1 mol甲烷的质量与0.5 mol O2的质量不相等 |
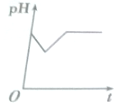
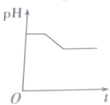
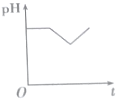
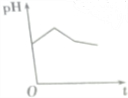
3.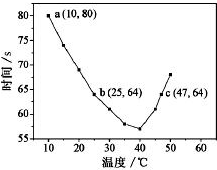 NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
 NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020mol•L-1NaHSO3溶液(含少量淀粉)10.0mL、KIO3(过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( )| A. | 40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反 | |
| B. | 当NaHSO3完全消耗时的离子方程式为:6HSO3-+2IO3-=6SO42-+2I-+6H+ | |
| C. | 图中a点对应的NaHSO3反应速率为5.5×10-5mol•L-1•s-1 | |
| D. | 温度高于40℃时,淀粉不宜用作该实验的指示剂 |
2.下列对化学反应的认识,不正确的是( )
| A. | 化学反应过程中,分子的种类和数目一定发生改变 | |
| B. | 化学反应涉及化学键的断裂和生成,而且还伴随着能量的变化 | |
| C. | 化学反应速率的大小主要取决于反应物的本身性质 | |
| D. | CO2(g)+C(s)?2CO(g)△H>0,△S>0,该反应常温下不能自发进行 |
1.标准状况下,5 mL O2和6 mL NO2在试管中组成混合气体,然后将试管倒立在水槽中,充分反应后,试管中剩余气体及其标准状况下的体积是( )
0 152316 152324 152330 152334 152340 152342 152346 152352 152354 152360 152366 152370 152372 152376 152382 152384 152390 152394 152396 152400 152402 152406 152408 152410 152411 152412 152414 152415 152416 152418 152420 152424 152426 152430 152432 152436 152442 152444 152450 152454 152456 152460 152466 152472 152474 152480 152484 152486 152492 152496 152502 152510 203614
| A. | 2.5 mL O2 | B. | 1.5 mL NO2 | C. | 2 mL NO | D. | 3.5 mL O2 |
 甲同学按如图所示装置做新制氯水受日光照射分解放出O2的验证实验,结果现象不明显.
甲同学按如图所示装置做新制氯水受日光照射分解放出O2的验证实验,结果现象不明显.