题目内容
9.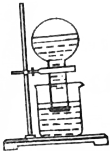 甲同学按如图所示装置做新制氯水受日光照射分解放出O2的验证实验,结果现象不明显.
甲同学按如图所示装置做新制氯水受日光照射分解放出O2的验证实验,结果现象不明显.(1)写出氯水受日光照射的化学方程式:2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑;
(2)乙同学反思了此实验的本质后,将新制氯水先在暗处存放3~4天,再拿出来做如图实验,结果效果十分明显.请解释乙同学实验取得成功的原理.
分析 (1)HClO不稳定,光照分解;
(2)次氯酸的浓度高低是决定本实验的现象是否明显的关键.
解答 解:(1)氯水受日光照射的化学方程式为2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,故答案为:2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑;
(2)将新制氯水先在暗处存放3~4天,促使氯水中存在的平衡H20+Cl2?HClO+HCl向右移,显然可提高次氯酸的浓度,光照时发生2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,效果十分明显,
答:平衡H20+Cl2?HClO+HCl向右移,显然可提高次氯酸的浓度.
点评 本题考查物质的性质,为高频考点,把握HClO的性质及化学平衡的移动为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
19.下列解释物质用途或现象的反应方程式不准确的是( )
| A. | NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO-3+Ba2++2OH-═BaCO3↓+2H2O+CO32- | |
| B. | Fe(NO3)3溶液中加入过量的HI溶液;2Fe3++2I-═2Fe2++I2 | |
| C. | Na2S203溶液中加入稀硫酸:S2O32-+2H+═SO2+S↓+H2O | |
| D. | 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+═Cl2↑+H2O |
20.化学与生活息息相关,下列说法正确的是( )
| A. | 下列生活用品主要由有机合成材料制成:羊毛衫、腈纶运动衣、涤纶连衣裙、纯棉T恤 | |
| B. | 不锈钢制作就是在普通钢中添加铬、镍等元素改变了钢铁内部结构,所以不锈钢是化合物 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 建筑业使用大量的沙,常使用内陆河的河沙及海洋的海沙 |
17.已知SO2+H2O2═H2SO4.将贮满干燥的某种气体的试管倒置于某种液体(括号内物质为液体,且液体足量)中,轻轻震荡,液体可以充满试管.该气体不可能是( )
| A. | HCl(澄清石灰水) | B. | NO2(H2O) | C. | SO2(H2O2溶液) | D. | Cl2(NaOH溶液) |
4.下列说法正确的是( )
| A. | 常温常压下,22.4L氮气所含原子数目大于2NA | |
| B. | 1 mol Na2O2跟H2O反应转移的电子数目为2NA | |
| C. | 标准状态下,22.4L三氧化硫所含分子数目大于NA | |
| D. | 1 mol甲烷的质量与0.5 mol O2的质量不相等 |
1.某盐溶液滴入氯水无明显现象,在滴入硝酸酸化的硝酸钡,有白色沉淀生成,则某盐可能是( )
| A. | MgCl2 | B. | FeSO4 | C. | Na2SO3 | D. | ZnSO4 |
4.有一包白色固体,可能含有KI、NaBr、BaCl2中的一种或两种物质.将白色物质溶入水得无色溶液,在该溶液中加入少量稀硫酸,有白色沉淀产生;在无色溶液中加入新制取的氯水,然后再滴入淀粉溶液,溶液变为蓝色.下列推断正确的是( )
| A. | 白色固体中既有KI,又有BaCl2 | B. | 白色固体中既有NaBr,又有BaCl2 | ||
| C. | 白色固体中可能有KI | D. | 白色固体中可能没有NaBr |
5.请在标有序号的空白处填空:
(1)利用催化剂可使NO和CO发生反应:2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0.已知增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面的表中.
①请填全表中的各空格;
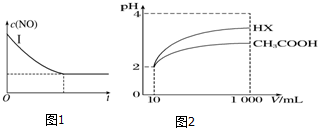
②实验Ⅰ中,NO的物质的量浓度(c)随时间(t)的变化如图所示.
请在给出的坐标图中画出实验Ⅱ、Ⅲ中NO的物质的量浓度(c)随时间(t)变化的曲线,并标明各曲线的实验编号.
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g) H=64.39KJ•mol-1
2H2O2(l)═2H2O(l)+O2(g) H=196.46KJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(l) H=-285.84KJ•mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-319.68kJ/mol.
(3)25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
①CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO.
②体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图2所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是稀释相同倍数,HX的pH变化比CH3COOH的大,酸性强,电离平衡常数大.
(4)①求常温下pH=2的H2SO4溶液中由H2O电离的c(H+)和c(OH-).
c(H+)=10-12mol•L-1,c(OH-)=10-12mol•L-1.
②在某温度时,测得0.01mol•L-1的NaOH溶液的pH=11.在此温度下,将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合.若所得混合液为中性,且a+b=12,则Va:Vb=10:1.
(1)利用催化剂可使NO和CO发生反应:2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0.已知增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面的表中.
①请填全表中的各空格;
| 实验 编号 | T(℃) | NO初始浓度 (mol•L-1) | CO初始浓度 (mol•L-1) | 催化剂的比表 面积(m2•g-1) |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 1.2×10-3 | 124 | ||
| Ⅲ | 350 | 82 |
请在给出的坐标图中画出实验Ⅱ、Ⅲ中NO的物质的量浓度(c)随时间(t)变化的曲线,并标明各曲线的实验编号.

(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g) H=64.39KJ•mol-1
2H2O2(l)═2H2O(l)+O2(g) H=196.46KJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)═H2O(l) H=-285.84KJ•mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-319.68kJ/mol.
(3)25℃时,部分物质的电离平衡常数如表所示:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平 衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
①CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为CH3COOH>H2CO3>HClO.
②体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000mL,稀释过程中pH变化如图2所示,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是稀释相同倍数,HX的pH变化比CH3COOH的大,酸性强,电离平衡常数大.
(4)①求常温下pH=2的H2SO4溶液中由H2O电离的c(H+)和c(OH-).
c(H+)=10-12mol•L-1,c(OH-)=10-12mol•L-1.
②在某温度时,测得0.01mol•L-1的NaOH溶液的pH=11.在此温度下,将pH=a的NaOH溶液Va L与pH=b的硫酸Vb L混合.若所得混合液为中性,且a+b=12,则Va:Vb=10:1.
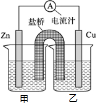 (1)已知下热化学方程式:
(1)已知下热化学方程式: