5.有四瓶澄清透明的溶液:①MgCl2溶液;②Cu(NO3)2溶液;③K2SO4溶液;④NaOH溶液.不用其他试剂即可将它们一一鉴别出来,鉴别出来的顺序是( )
| A. | ④②①③ | B. | ①④③② | C. | ②③①④ | D. | ②④①③ |
4.下列关于钠的叙述正确的是( )
| A. | 钠在空气中露置会立刻被空气氧化成过氧化钠 | |
| B. | 钠单质具有强还原性,可将铜从其盐溶液中置换出来 | |
| C. | 钠与钠离子都具有强的还原性 | |
| D. | 钠与稀盐酸反应的实质是与氢离子的反应 |
2.下列离子方程式书写正确的( )
| A. | Na2CO3溶液中通入少量SO2:SO2+H2O+2CO32-═SO32-+2HCO3- | |
| B. | 漂白粉中滴加浓盐酸加热制取氯气:ClO-+Cl-+2H+ $\frac{\underline{\;\;△\;\;}}{\;}$ Cl2+H2O | |
| C. | 将0.1mol•L-1的NH4Al(SO4)2溶液与0.2mol•L-1的Ba(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═AlO2-↓+2BaSO4↓+2H2O | |
| D. | 含0.4molFeI2的溶液中通入0.3mol氯气:4Fe2++2I-+3Cl2═4Fe3++I2+6Cl- |
20.某研究性学习小组为探究二氧化硫的还原性,查阅到如表资料:
根据上述资料,请你参与以下探究:
(1)写出铜与浓硫酸反应的化学方程式Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)把足量SO2通入适量的碘水中,可能观察到的现象是溶液棕黄色褪去;
(3)证明SO2被氧化为SO42-所使用的试剂是盐酸和BaCl2溶液;
(4)如果该探究小组想利用上述原理除去CO2中的SO2,并检验是否除尽,下列方案可行的是AB(填字母)
A、将混合气体通过碘水,再通过品红溶液
B、将混合气体通过氯化钡和过氧化氢的混合溶液,再通过碘水溶液
C、将混合气体通过NaOH溶液,再通过品红溶液
D、将混合气体通过浓硫酸溶液,再通过品红溶液
(5)若该探究小组就上述实验提出,把含+4价硫元素化合物转化为含+6价硫元素化合物,下列试剂可以实现上述转化的是ABC(填字母)
A、氧气 B、MnO4- C、氯气 D、浓硫酸.
| 资料卡 NO:2006-KI-001 主题:二氧化硫的还原性 ①课本上:向二氧化硫水溶液中滴加BaCl2溶液,再滴加0.5mL3%的过氧化氢溶液,振荡片刻后滴加稀盐酸,有白色沉淀生成 ②《无机化学》下册,P658:亚硫酸是较强的还原剂,可以将Cl2、I2、MnO4-还原为Cl-、I-、Mn2+,如: H2SO3+I2+H2O═H2SO4+2HI |
(1)写出铜与浓硫酸反应的化学方程式Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)把足量SO2通入适量的碘水中,可能观察到的现象是溶液棕黄色褪去;
(3)证明SO2被氧化为SO42-所使用的试剂是盐酸和BaCl2溶液;
(4)如果该探究小组想利用上述原理除去CO2中的SO2,并检验是否除尽,下列方案可行的是AB(填字母)
A、将混合气体通过碘水,再通过品红溶液
B、将混合气体通过氯化钡和过氧化氢的混合溶液,再通过碘水溶液
C、将混合气体通过NaOH溶液,再通过品红溶液
D、将混合气体通过浓硫酸溶液,再通过品红溶液
(5)若该探究小组就上述实验提出,把含+4价硫元素化合物转化为含+6价硫元素化合物,下列试剂可以实现上述转化的是ABC(填字母)
A、氧气 B、MnO4- C、氯气 D、浓硫酸.
17.常温下,浓度均为0.1mol/L的6种溶液的pH如下表:
(1)上述溶液中的阴离子结合H +能力最弱的为CO32-(填阴离子化学式)
(2)NaAlO 2溶液呈碱性的原因是AlO2-+2H2O?Al(OH)3+OH-(用离子方程式表示).将溶液加热蒸干最后得到的固体产物是NaAlO2;
(3)结合表中数据分析,与0.1mol/L的CH 3COONa溶液中水的电离程度相同的有BE(填字母代号).
A.pH=8.8的NaOH溶液 B.pH=5.2的NH 4Cl溶液 C.pH=5.2的盐酸
D.0.1mol/L的NaCN溶液 E.pH=8.8的Na 2CO 3溶液
(4)将浓度均为0.1mol/L的b、c等体积混合,所得溶液中各离子浓度关系正确的有BDE.
A.c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
B.2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3)
C.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D.c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
E.c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
F.c(Na+)>c(CO32-)>c(HCO3-)>c(H+)>c(OH-)
(5)0.2mol/LHCl与0.1mol/L NaAlO 2溶液等体积混合溶液后离子浓度顺序为c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-).
0 152141 152149 152155 152159 152165 152167 152171 152177 152179 152185 152191 152195 152197 152201 152207 152209 152215 152219 152221 152225 152227 152231 152233 152235 152236 152237 152239 152240 152241 152243 152245 152249 152251 152255 152257 152261 152267 152269 152275 152279 152281 152285 152291 152297 152299 152305 152309 152311 152317 152321 152327 152335 203614
| 序号 | a | b | c | d | e | f |
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | NaAlO2 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
(2)NaAlO 2溶液呈碱性的原因是AlO2-+2H2O?Al(OH)3+OH-(用离子方程式表示).将溶液加热蒸干最后得到的固体产物是NaAlO2;
(3)结合表中数据分析,与0.1mol/L的CH 3COONa溶液中水的电离程度相同的有BE(填字母代号).
A.pH=8.8的NaOH溶液 B.pH=5.2的NH 4Cl溶液 C.pH=5.2的盐酸
D.0.1mol/L的NaCN溶液 E.pH=8.8的Na 2CO 3溶液
(4)将浓度均为0.1mol/L的b、c等体积混合,所得溶液中各离子浓度关系正确的有BDE.
A.c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
B.2c(Na+)=3c(CO32-)+3c(HCO3-)+3c(H2CO3)
C.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D.c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
E.c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
F.c(Na+)>c(CO32-)>c(HCO3-)>c(H+)>c(OH-)
(5)0.2mol/LHCl与0.1mol/L NaAlO 2溶液等体积混合溶液后离子浓度顺序为c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-).
 ,AE3的分子立体构型为三角锥形;AE3分子在潮湿空气中能水解生成一种常用的漂白剂X和一种能使紫色石蕊变蓝色的气体Y,完成反应方程式:NCl3+3H2O=3HClO+NH3.
,AE3的分子立体构型为三角锥形;AE3分子在潮湿空气中能水解生成一种常用的漂白剂X和一种能使紫色石蕊变蓝色的气体Y,完成反应方程式:NCl3+3H2O=3HClO+NH3.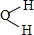 .
. ,A的结构式H-C≡C-H
,A的结构式H-C≡C-H 反应类型加聚反应;F生成B化学方程式HCl+CH2=CH2→CH3CH2Cl;
反应类型加聚反应;F生成B化学方程式HCl+CH2=CH2→CH3CH2Cl; 铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
铁及其化合物在生活、生产中有广泛应用.请回答下列问题: 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.