题目内容
18. 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.(1)在如图所示仪器中,配制上述溶液肯定不需要的是A、C(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是烧杯、玻璃棒、500mL容量瓶.
(2)在容量瓶的使用方法中,下列操作不正确的是B、C、D
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线.
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线.
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀.
(3)根据计算用托盘天平称取的质量为2.0g.在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度小于0.1mol/L(填“大于”“小于”或“等于”).
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为
13.6mL,如果实验室有15mL、20mL、50mL量筒,应选用15mL量筒最好.
分析 (1)依据配制一定物质的量浓度溶液的一般步骤选择需要的仪器,判断用不到的仪器和缺少的仪器;
(2)容量瓶是一种精密仪器,容积会随着温度的改变而改变,故不能受热,不能用来溶解固体、稀释浓溶液,不能用来长期存在溶液,在使用前应查漏,据此分析;
(3)依据m=CVM计算需要溶质的质量;在实验中其他操作均正确,若定容时仰视刻度线,导致溶液体积偏小,依据C=$\frac{n}{V}$判断;
(4)依据c=$\frac{1000ρω}{M}$计算浓H2SO4的物质的量浓度,再根据溶液稀释前后物质的量不变计算所需浓硫酸的体积;
依据所需浓硫酸的体积选择合适的量筒.
解答 解:(1)配制一定物质的量浓度溶液的一般步骤:计算、称量或者量取、溶解或者稀释、移液、洗涤、定容、摇匀,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以用不到的仪器:平底烧瓶、分液漏斗;还缺少的仪器:烧杯、玻璃棒、500mL容量瓶;
故答案为:A、C; 烧杯、玻璃棒、500mL容量瓶;
(2)A.容量瓶是带有活塞的仪器,使用前要检查是否漏水,故A正确;
B.容量瓶用蒸馏水洗净后,不能够使用待配溶液润洗,否则导致配制的溶液浓度偏高,故B错误;
C.容量瓶是精密定量仪器,只能用于配制一定物质的量浓度的溶液,不能用于溶解,应该在烧杯中溶解固体,故C错误;
D.容量瓶是精密定量仪器,只能用于配制一定物质的量浓度的溶液,不能用于稀释浓溶液,应该在烧杯中稀释浓溶液,故D错误;
E.摇匀的正确操作为:盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次,故E正确;
故选:BCD;
(3)需要0.1mol/LNaOH溶液450mL,应选择500mL容量瓶,实际配制500mL溶液,需要溶质的质量=0.1mol/L×0.5L×40g/mol=2.0g;若定容时仰视刻度线,导致溶液体积偏小,依据C=$\frac{n}{V}$可知所配溶液浓度偏低;
故答案为:2.0; 小于;
(4)浓H2SO4的物质的量浓度c=$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,稀释前后溶质的物质的量不变,设需要浓硫酸的体积为V,则:V×18.4mol/L=500mL×0.5mol/L,解得V=13.6ml;
故答案为:13.6;15.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和操作步骤是解题关键,注意容量瓶的正确使用方法,题目难度不大.

| A. | 元素X只能形成一种氢化物 | |
| B. | 原子半径的大小顺序:r(W)>r(Z)>r(X)>r(Y) | |
| C. | 化合物Q中存在两种类型的共价键 | |
| D. | X与Z形成的化合物在熔融状态下能导电 |
| A. | 78g过氧化钠晶体中,含3NA个离子 | |
| B. | 常温常压下,22.4L氦气含有NA个氦原子 | |
| C. | 在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA | |
| D. | 常温下16g O2与O3的混合气体中含氧原子数为NA |

| A. | 柠檬烯的分子式为C10H14 | |
| B. | 它的一氯代物有8种 | |
| C. | 它和丁基苯互为同分异构体 | |
| D. | 一定条件下,它分别可以发生加成、取代、氧化反应,但不能发生还原反应 |
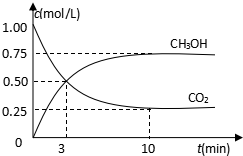 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在485℃时,在体积为1L的密闭容器中,充入1ol CO2和3mol H2,一定条件下发生反应合成甲醇:
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在485℃时,在体积为1L的密闭容器中,充入1ol CO2和3mol H2,一定条件下发生反应合成甲醇: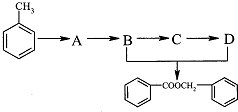
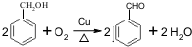
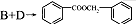 的化学方程式为
的化学方程式为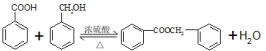
 ,AE3的分子立体构型为三角锥形;AE3分子在潮湿空气中能水解生成一种常用的漂白剂X和一种能使紫色石蕊变蓝色的气体Y,完成反应方程式:NCl3+3H2O=3HClO+NH3.
,AE3的分子立体构型为三角锥形;AE3分子在潮湿空气中能水解生成一种常用的漂白剂X和一种能使紫色石蕊变蓝色的气体Y,完成反应方程式:NCl3+3H2O=3HClO+NH3.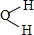 .
.