19.相同温度下等物质的量浓度的下列溶液中,pH值最大的是 ( )
| A. | NH4Cl | B. | NH3.H2O | C. | NH4HSO4 | D. | (NH4)2SO4 |
18.2015年8月12日晚11时许,天津市塘沽开发区危险品仓库发生大爆炸,据悉,该危险品仓库存放的危险品有多种,包括剧毒化学品氰化钠(NaCN).现场火光冲天.据多位市民反映,事发时十公里范围内均有震感,抬头可见蘑菇云,截至今日,已近150人遇难.安全问题再次敲响了警钟.下列关于安全问题的说法,不正确的是( )
| A. | 简单辨认有味的化学药品时,将瓶口远离鼻子,用手在瓶口上方扇动,稍闻其味即可 | |
| B. | 处置实验过程产生的剧毒药品废液,稀释后用大量水冲净 | |
| C. | 可用强氧化剂如H2O2等将NaCN氧化为无毒物质 | |
| D. | 危险化学品包括:爆炸品、易燃物质、自燃自热物质、氧化性气体等 |
17.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1mol甲醇中含有C-H键的数目为4NA | |
| B. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 0.1mol的CaC2中含阴离子数是0.1NA | |
| D. | 1L 0.1mol•L-1的NaHCO3溶液中HCO${\;}_{3}^{-}$和CO${\;}_{3}^{2-}$离子数之和为0.1NA |
16.下列不能达到实验目的是( )
| A. | 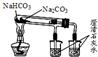 比较苏打和小苏打的热稳定性 比较苏打和小苏打的热稳定性 | B. | 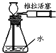 检查装置气密性 检查装置气密性 | ||
| C. |  向容量瓶转移液体 向容量瓶转移液体 | D. | 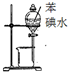 用苯从碘水中分离出碘 |
15.在花瓶中加入“营养液”,能延长鲜花的寿命.下表是500mL“营养液”中含有的成分,阅读后回答下列问题:
(1)下列“营养液”的成分中,属于非电解质的是A.(填序号)
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“营养液”中K+(阿司匹林中不含K+)的物质的量浓度为$\frac{\frac{0.5}{158}+\frac{0.5}{174}×2}{0.5}$ mol•L-1(只要求写表达式,不用写出计算结果).
(3)配制上述“营养液”500mL所需的仪器有:电子天平、药匙、烧杯、500ml容量瓶、玻璃棒、胶头滴管.(在横线上填写所缺仪器的名称)
(4)在配制一定物质的量浓度的溶液时,一般可分为以下几个步骤:①称量②计算③溶解
④摇匀⑤转移⑥洗涤⑦定容⑧冷却.其正确的操作顺序为②①③⑧⑤⑥⑦④.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BC,使所配制溶液的浓度偏高的是A,偏低的是DE.
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
D.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
E.定容时发现液面高于容量瓶的刻度线,倒出一部分液体后再加蒸馏水至刻度线.
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 50.0 | 342 |
| 硫酸钾 | 0.5 | 174 |
| 阿司匹林 | 0.4 | 180 |
| 高锰酸钾 | 0.5 | 158 |
| 硝酸银 | 0.2 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“营养液”中K+(阿司匹林中不含K+)的物质的量浓度为$\frac{\frac{0.5}{158}+\frac{0.5}{174}×2}{0.5}$ mol•L-1(只要求写表达式,不用写出计算结果).
(3)配制上述“营养液”500mL所需的仪器有:电子天平、药匙、烧杯、500ml容量瓶、玻璃棒、胶头滴管.(在横线上填写所缺仪器的名称)
(4)在配制一定物质的量浓度的溶液时,一般可分为以下几个步骤:①称量②计算③溶解
④摇匀⑤转移⑥洗涤⑦定容⑧冷却.其正确的操作顺序为②①③⑧⑤⑥⑦④.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BC,使所配制溶液的浓度偏高的是A,偏低的是DE.
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
D.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
E.定容时发现液面高于容量瓶的刻度线,倒出一部分液体后再加蒸馏水至刻度线.
14.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 12.0g熔融的NaHSO4中含有的阳离子数为0.2NA | |
| B. | 标准状况下,0.1molCl2溶于水,转移电子数目为0.1NA | |
| C. | 1molCO2与含1molNaOH的溶液反应后溶液中HCO3-数为NA | |
| D. | 标准状况下,2.24LNH3和CH4的混合气体,所含电子总数为NA |
13.下列有关说法正确的是( )
| A. | 若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 | |
| B. | 一定条件下反应N2+3H22?NH3达到平衡时,3v正(H2)=2v逆(NH3) | |
| C. | 酸碱质子理论认为,凡能给出质子(H+) 的物质都是酸,凡能接受质子的物质都是碱.根据这一理论,Al(OH)3、NaHCO3都是两性物质 | |
| D. | 对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
10. 在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
(1)该反应在60S内用NO2的表示的反应速率为0.002 mol•L-1•s-1.
(2)下表是不同温度下测定得到的该反应的化学平衡常数.
据此可推测该反应(生成NO2)是吸热反应(填“吸热”或“放热”). 升高温度,平衡向正反应方向移动(填“正反应”或“逆反应”).
0 152040 152048 152054 152058 152064 152066 152070 152076 152078 152084 152090 152094 152096 152100 152106 152108 152114 152118 152120 152124 152126 152130 152132 152134 152135 152136 152138 152139 152140 152142 152144 152148 152150 152154 152156 152160 152166 152168 152174 152178 152180 152184 152190 152196 152198 152204 152208 152210 152216 152220 152226 152234 203614
 在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)(1)该反应在60S内用NO2的表示的反应速率为0.002 mol•L-1•s-1.
(2)下表是不同温度下测定得到的该反应的化学平衡常数.
| T/K | 323 | 373 |
| K值 | 0.022 | ? |
 工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g).
工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g).