17.已知:还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入NaIO3溶液.加入NaIO3的物质的量和和析出的I2的物质的量的关系曲线如图.下列说法正确的是( )

| A. | 反应过程中的氧化产物均为SO3 | |
| B. | a点时消耗NaHSO3的物质的量为1.0 mol | |
| C. | 0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-=3SO42-+I-+3H+ | |
| D. | 当溶液中I?与I2的物质的量之比为1:1时,加入的NaIO3为1.2 mol |
16.下列鉴别物质的方法能达到目的是( )
| A. | 用Br2的CCl4溶液鉴别CH2=CH2和HC≡CH | |
| B. | 用AgNO3溶液鉴别KCl溶液和MgCl2溶液 | |
| C. | 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 | |
| D. | 用酚酞溶液鉴别未知浓度的NaOH溶液和Na2CO3溶液 |
14.钾.钠合金(含50%~80%钾),可作原子反应堆的导热剂,下面有关该合金的事实与此应用无关的是( )
| A. | 熔点260.7K | B. | 具有很高的比热 | C. | 可作冷却剂 | D. | 能跟水剧烈反应 |
13.可用作磁性材料的物质是( )
| A. | FeO | B. | Fe2O3 | C. | Fe3O4 | D. | FeS |
11.用含有A1203.SiO2和少量FeO•xFe2O3的铝灰制备A12(SO4)3•18H2O.工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩.结晶.分离,得到产品.
(1)H2S04溶解A1203的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)KMnO4-氧化Fe2+的离子方程式补充完整:
1MnO4-+5Fe2++8H+=1Mn2++5Fe3++4H2O
(3)已知:
生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol•L-1
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnS04的目的是除去过量的MnO4-.
0 151979 151987 151993 151997 152003 152005 152009 152015 152017 152023 152029 152033 152035 152039 152045 152047 152053 152057 152059 152063 152065 152069 152071 152073 152074 152075 152077 152078 152079 152081 152083 152087 152089 152093 152095 152099 152105 152107 152113 152117 152119 152123 152129 152135 152137 152143 152147 152149 152155 152159 152165 152173 203614
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩.结晶.分离,得到产品.
(1)H2S04溶解A1203的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)KMnO4-氧化Fe2+的离子方程式补充完整:
1MnO4-+5Fe2++8H+=1Mn2++5Fe3++4H2O
(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnS04的目的是除去过量的MnO4-.
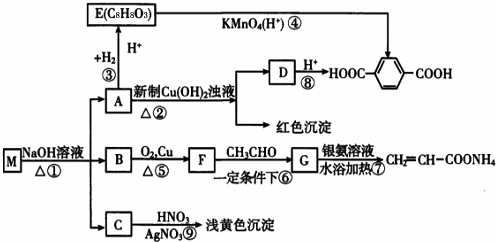
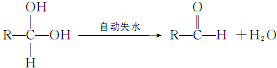
 ;E:
;E: ;G:CH2=CHCHO.
;G:CH2=CHCHO. .
. (写一种).
(写一种).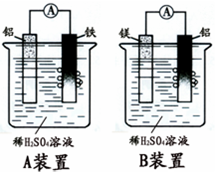 有甲.乙两位学生分别利用如图A,B装置的原电池反应检测金属的活动性顺序,
有甲.乙两位学生分别利用如图A,B装置的原电池反应检测金属的活动性顺序,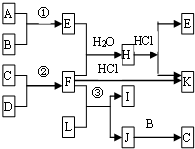 如图是部分短周期元素的单质及其化合物的转化关系图
如图是部分短周期元素的单质及其化合物的转化关系图