9.阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池反应为:2H2+O2═2H2O,电解液为KOH,反应保持在较高温度,使H2O蒸发,下列叙述正确的是( )
| A. | 电池能发出蓝色火焰 | B. | H2为正极,O2为负极 | ||
| C. | 正极反应为:O2+2H2O+4e-═4OH- | D. | 正极反应为:2H2+4OH--4e-═4H2O |
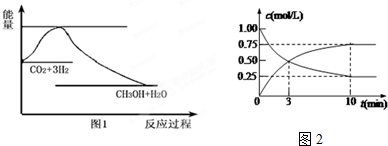
8.甲醇属于再生能源,可代替汽油作为汽车燃料.下列能正确表示甲醇燃烧热的热化学方程式为( )
| A. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l);△H=+763.3kJ•mol-1 | |
| B. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l);△H=-763.3kJ•mol-1 | |
| C. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(g);△H=-675.3kJ•mol-1 | |
| D. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l);△H=-1526.6kJ•mol-1 |
7.实验室制取氢氧化铝,最好选用( )
| A. | 铝与氢氧化钠溶液反应 | B. | 铝与水反应 | ||
| C. | 氯化铝溶液与氢氧化钠溶液反应 | D. | 氯化铝溶液与氨水反应 |
6.固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,它与水反应的化学方程式为:NH5+H2O→NH3•H2O+H2↑,则下列有关说法正确的是( )
| A. | 1mol NH5中含有5NA个N-H键(NA为阿伏加德罗常数) | |
| B. | NH5中既有共价键,又有离子键 | |
| C. | NH5的电子式为: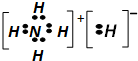 | |
| D. | 与水反应时,水作氧化剂,生成1mol氢气,转移2mol电子 |
4.下列各项中物质的类别和用途对应关系不正确的是( )
| A | B | C | D |
| A12O3 | Si | Na2O2 | Na2SiO3 |
| 两性氧化物 | 单质 | 碱性氧化物 | 正盐 |
| 工业用电解法冶炼铝 | 制作太阳能电池 | 用于呼吸面具作为氧气的来源 | 制备硅胶 |
| A.A | B.B | C.C | D.D |
3.毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2•2H2O的流程如图:

(1)毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而使反应速率加快;直接蒸干BaCl2溶液能(填“能”或“不能”)得到BaCl2•2H2O晶体.
(2)
加入NH3•H2O调节pH=8可除去Fe3+(填离子符号),滤渣Ⅱ中含Mg(OH)2、Ca(OH)2(填化学式).加入H2C2O4时应避免过量,原因是H2C2O4过量会导致生成BaC2O4沉淀,产品的产量减少.
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9.
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行.
已知:2CrO42-+2H+═Cr2O72-+H2O Ba2++CrO42-═BaCrO4↓
步骤Ⅰ移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL.
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL.BaCl2溶液的浓度为$\frac{b(V0-V1)}{y}$mol•L-1.

(1)毒重石用盐酸浸取前需充分研磨,目的是增大接触面积从而使反应速率加快;直接蒸干BaCl2溶液能(填“能”或“不能”)得到BaCl2•2H2O晶体.
(2)
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9.
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行.
已知:2CrO42-+2H+═Cr2O72-+H2O Ba2++CrO42-═BaCrO4↓
步骤Ⅰ移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL.
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL.BaCl2溶液的浓度为$\frac{b(V0-V1)}{y}$mol•L-1.
20.26g锌和含63gHNO3的稀硝酸正好完全反应,生成的还原产物的相对分子质量可能是( )
0 151903 151911 151917 151921 151927 151929 151933 151939 151941 151947 151953 151957 151959 151963 151969 151971 151977 151981 151983 151987 151989 151993 151995 151997 151998 151999 152001 152002 152003 152005 152007 152011 152013 152017 152019 152023 152029 152031 152037 152041 152043 152047 152053 152059 152061 152067 152071 152073 152079 152083 152089 152097 203614
| A. | 80 | B. | 30 | C. | 46 | D. | 28 |