题目内容
7.实验室制取氢氧化铝,最好选用( )| A. | 铝与氢氧化钠溶液反应 | B. | 铝与水反应 | ||
| C. | 氯化铝溶液与氢氧化钠溶液反应 | D. | 氯化铝溶液与氨水反应 |
分析 由于氢氧化铝能溶于过量的强碱,所以实验室用可溶性的铝盐与氨水反应制备氢氧化铝.
解答 解:由于氢氧化铝能溶于过量的强碱,所以实验室用可溶性的铝盐与氨水反应制备氢氧化铝,则氯化铝溶液与氨水反应可以制得氢氧化铝,故D正确;
故选D.
点评 本题考查了氢氧化铝的制备,把握铝及其化合物的性质是解答该题的关键,题目难度不大.

练习册系列答案
相关题目
17.同温同压下,下列气体的密度最大的是( )
| A. | 氢气 | B. | 二氧化硫 | C. | 氧气 | D. | 二氧化碳 |
18.氢氧化铁胶体区别于FeCl3溶液最本质的特征( )
| A. | Fe(OH)3胶体粒子的直径在1~100 nm之间 | |
| B. | Fe(OH)3胶体具有丁达尔效应 | |
| C. | Fe(OH)3胶体是均一的分散系 | |
| D. | Fe(OH)3胶体的分散质能通过滤纸 |
12.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在46 gN02和N204的混合物气体中所含原子总数为3NA个 | |
| B. | 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| C. | 2.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.04NA | |
| D. | 7.8g过氧化钠与足量CO2反应,转移电子数为0.2NA,CO2为还原剂 |
19.氯气是一种化学性质很活泼的单质,它具有较强的氧化性,下列叙述中不正确的是( )
| A. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 | |
| B. | 纯净的H2在Cl2中安静地燃烧,发出苍白色火焰 | |
| C. | 氯气通入品红溶液中,溶液会褪色,是因为氯气具有漂白性 | |
| D. | 氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸 |
16.下列物质中既能与稀H2SO4反应,又能与NaOH溶液反应的是:( )
①Al ②Fe3O4③NaHCO3 ④Al(OH)3⑤Na2CO3.
①Al ②Fe3O4③NaHCO3 ④Al(OH)3⑤Na2CO3.
| A. | ①②④ | B. | ②③⑤ | C. | ②④⑤ | D. | ①③④ |
17.铝--空气电池可用作水下动力电源,其原理如图所示.下列有关铝--空气电池的说法中正确的是( )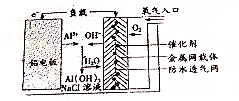

| A. | 电池的负极材料为附着有催化剂的金属网载体 | |
| B. | 电池负极的电极反应为2Cl-2e-═Cl2↑ | |
| C. | 铝电池的电极反应为Al-3e-═Al3+ | |
| D. | 正极的电极反应为O2+4H++4e-═2H2O |