9.下列叙述正确的是( )
| A. | 氯化钠的电离是指在电流作用下离解成钠离子和氯离子 | |
| B. | 溶于水后能电离出氢离子的化合物都是酸 | |
| C. | 硫酸钡难溶于水,所以硫酸钡属于弱电解质 | |
| D. | 醋酸溶液中存在H+、CH3COOH、CH3COO-等微粒,故醋酸是弱电解质 |
7.下列物质的熔点均按由高到低的次序排列,其原因是由于键能由大到小排列的是( )
| A. | 钠、干冰 | B. | 金刚石、晶体硅 | ||
| C. | 碘化氢、溴化氢 | D. | 二氧化硅、二氧化碳 |
6.锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性.锂离子电池放电时的电极反应式为:
负极反应:C6Li-xe-═C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成复合材料)
正极反应:Li1-xMO2+xLi++x e-═LiMO2(LiMO2表示含锂的过渡金属氧化物)
下列有关说法正确的是( )
负极反应:C6Li-xe-═C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成复合材料)
正极反应:Li1-xMO2+xLi++x e-═LiMO2(LiMO2表示含锂的过渡金属氧化物)
下列有关说法正确的是( )
| A. | 锂离子电池充电时电池反应为C6Li+Li1-xMO2═LiMO2+C6Li1-x | |
| B. | 电池反应中,锂、锌、银、铅各失去1mol电子,金属锌所消耗的质量最小 | |
| C. | 锂离子电池放电时电池内部Li+向负极移动 | |
| D. | 锂离子电池充电时阴极反应为C6Li1-x+xLi++x e-═C6Li |
5.已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S:Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是( )
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S:Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是( )
| A. | CuS<Cu(OH)2<CuCO3 | B. | CuCO3<Cu(OH)2<CuS | C. | CuS<CuCO3<Cu(OH)2 | D. | Cu(OH)2<CuCO3<CuS |
1.下列表示式错误的是( )
| A. | Mg2+的电子排布图: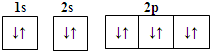 | B. | Na+的结构示意图: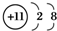 | ||
| C. | Cr的价层电子排布式:3d54s1 | D. | C的电子排布式:1s22s12p3 |
20.酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据下表所示:溶解度/(g/100g水)
回答下列问题:
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为2MnO2+Zn+2H+=2MnOOH+Zn2+2MnO2+Zn+2H+=2MnOOH+Zn2+.
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn0.05g.(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过加热浓缩、冷却结晶分离回收;滤渣的主要成分是MnO2、MnOOH和碳粉,欲从中得到较纯的MnO2,最简便的方法是在空气中加热,其原理是碳粉转变为二氧化碳,MnOOH氧化为二氧化锰.
(4)已知25℃时:SO2(g)+2CO(g)=2CO2(g)+$\frac{1}{x}$Sx(s)△H=akJ/mol
2COS(g)+SO2(g)=2CO2(g)+$\frac{3}{x}$Sx(s)△H=b kJ/mol.
则CO与Sx生成COS反应的热化学方程式是xCO(g)+Sx(s)=xCOS(g)△H=-0.5x(b-a)kJ/mol.
0 151885 151893 151899 151903 151909 151911 151915 151921 151923 151929 151935 151939 151941 151945 151951 151953 151959 151963 151965 151969 151971 151975 151977 151979 151980 151981 151983 151984 151985 151987 151989 151993 151995 151999 152001 152005 152011 152013 152019 152023 152025 152029 152035 152041 152043 152049 152053 152055 152061 152065 152071 152079 203614
| 温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 45.8 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 452 | 488 | 614 |
(1)该电池的正极反应式为MnO2+H++e-=MnOOH,电池反应的离子方程式为2MnO2+Zn+2H+=2MnOOH+Zn2+2MnO2+Zn+2H+=2MnOOH+Zn2+.
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn0.05g.(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过加热浓缩、冷却结晶分离回收;滤渣的主要成分是MnO2、MnOOH和碳粉,欲从中得到较纯的MnO2,最简便的方法是在空气中加热,其原理是碳粉转变为二氧化碳,MnOOH氧化为二氧化锰.
(4)已知25℃时:SO2(g)+2CO(g)=2CO2(g)+$\frac{1}{x}$Sx(s)△H=akJ/mol
2COS(g)+SO2(g)=2CO2(g)+$\frac{3}{x}$Sx(s)△H=b kJ/mol.
则CO与Sx生成COS反应的热化学方程式是xCO(g)+Sx(s)=xCOS(g)△H=-0.5x(b-a)kJ/mol.
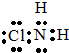 ,从物质结构的角度解释两者熔点相差较大的原因氯胺NH2Cl为分子晶体,NH4Cl为离子晶体,熔沸点离子晶体高于分子晶体.
,从物质结构的角度解释两者熔点相差较大的原因氯胺NH2Cl为分子晶体,NH4Cl为离子晶体,熔沸点离子晶体高于分子晶体.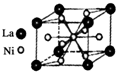 目前,利用金属或合金储氢已取得很大进展,先后发现了Ni、Mg、Fe基三个系列的储氢材料,如图是一种储氢密度超过液氢的镍基合金的晶胞结构图.
目前,利用金属或合金储氢已取得很大进展,先后发现了Ni、Mg、Fe基三个系列的储氢材料,如图是一种储氢密度超过液氢的镍基合金的晶胞结构图.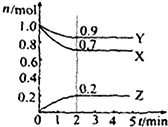 某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如图所示,图中数据分析:
某温度时在2L容器中X、Y、Z三种物质的物质的量(n)随时间(t)变化的曲线如图所示,图中数据分析: