题目内容
6.锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性.锂离子电池放电时的电极反应式为:负极反应:C6Li-xe-═C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成复合材料)
正极反应:Li1-xMO2+xLi++x e-═LiMO2(LiMO2表示含锂的过渡金属氧化物)
下列有关说法正确的是( )
| A. | 锂离子电池充电时电池反应为C6Li+Li1-xMO2═LiMO2+C6Li1-x | |
| B. | 电池反应中,锂、锌、银、铅各失去1mol电子,金属锌所消耗的质量最小 | |
| C. | 锂离子电池放电时电池内部Li+向负极移动 | |
| D. | 锂离子电池充电时阴极反应为C6Li1-x+xLi++x e-═C6Li |
分析 A.充电时电池反应式为放电电池反应式相反;
B.根据m=nM计算其质量;
C.放电时,电池内部阳离子向正极移动,阴离子向负极移动;
D.充电时,阴极上得电子发生还原反应,与放电时负极电极反应式相反.
解答 解:A.充电时电池反应式为放电电池反应式相反,放电时电池反应式为C6Li+Li1-xMO2=C6Li1-x+LiMO2,则充电时电池反应式为C6Li1-x+LiMO2=C6Li+Li1-xMO2,故A错误;
B.电池反应中,锂、锌、银、铅各失去1 mol 电子,消耗这几种金属的物质的量分别是1mol、0.5mol、1mol、0.5mol,根据m=nM知,消耗其质量分别是7g、32.5g、108g、103.5g,所以消耗Li质量最小,比能量最大,故B错误;
C.放电时,电池内部阳离子向正极移动,阴离子向负极移动,所以Li+向正极移动,故C错误;
D.充电时,阴极上得电子发生还原反应,与放电时负极电极反应式相反,则电极反应式为C6Li1-x+xLi++xe-═C6Li,故D正确;
故选D.
点评 本题考查原电池和电解池原理,明确蓄电池中正负极与阳极、阴极电极反应式关系是解本题关键,结合电池内部阴阳离子移动方向即可解答,题目难度不大.

练习册系列答案
相关题目
16.X、Y、Z、W为四种常见的短周期元素.其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如图所示:
请回答下列问题:
(1)W位于周期表中第三周期,第VIIA族.
(2)X和氢可以构成+1价阳离子,其电子式是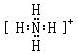 ,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).
,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为2S2Cl2+2H2O═3S↓+SO2↑+4HCl.
(4)①Y和Z可组成一种气态化合物Q,Q能与W的单质在潮湿环境中反应,反应的化学方程式是SO2+Cl2+2H2O=2HCl+H2SO4.
②在一定条件下,化合物Q与Y的单质反应达平衡时有三种气态物质,反应时,每转移4mol电子放热190.0kJ,该反应的热化学方程式是2SO2 (g)+O2(g)?2SO3(g)△H=-190.0 kJ•mol-1.
| X | Y | |
| Z | W |
(1)W位于周期表中第三周期,第VIIA族.
(2)X和氢可以构成+1价阳离子,其电子式是
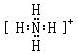 ,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).
,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为2S2Cl2+2H2O═3S↓+SO2↑+4HCl.
(4)①Y和Z可组成一种气态化合物Q,Q能与W的单质在潮湿环境中反应,反应的化学方程式是SO2+Cl2+2H2O=2HCl+H2SO4.
②在一定条件下,化合物Q与Y的单质反应达平衡时有三种气态物质,反应时,每转移4mol电子放热190.0kJ,该反应的热化学方程式是2SO2 (g)+O2(g)?2SO3(g)△H=-190.0 kJ•mol-1.
17.下列化合物中同分异构体数目(不考虑立体异构)最少的是( )
| A. | 分子式为C5H12的烃 | B. | 分子式为C4H10O的醇 | ||
| C. | 分子式为C4H8的烯烃 | D. | 分子式为C3H6O2的酯 |
1.下列表示式错误的是( )
| A. | Mg2+的电子排布图: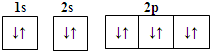 | B. | Na+的结构示意图: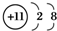 | ||
| C. | Cr的价层电子排布式:3d54s1 | D. | C的电子排布式:1s22s12p3 |
18.过氧化钠具有强氧化性.下列说法不正确的是( )
| A. | 过氧化钠与二氧化硫反应时可生成硫酸钠 | |
| B. | 1mol过氧化钠中阴离子数目约为6.02×1023 | |
| C. | Na2O2与CO2反应时,Na2O2是氧化剂CO2是还原剂 | |
| D. | 将等物质的量的Na2O和Na2O2分别溶于等质量的足量水中所得溶液的质量相等 |
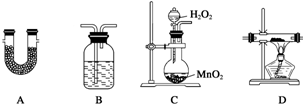
16.如图所示的四种实验操作对应描述正确的是( )
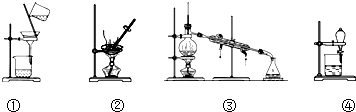

| A. | 除去KCl溶液中的K2CO3,加入适量Ca(NO3)2溶液,再用①装置分离 | |
| B. | 用②装置除去自来水中的Cl-等杂质 | |
| C. | 回收碘的CCl4溶液中的CCl4,可选用③装置 | |
| D. | 分离水和植物油,选用④装置,下层的植物油可从分液漏斗的下层放出 |

 (或
(或
 ).
).