题目内容
3.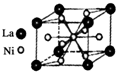 目前,利用金属或合金储氢已取得很大进展,先后发现了Ni、Mg、Fe基三个系列的储氢材料,如图是一种储氢密度超过液氢的镍基合金的晶胞结构图.
目前,利用金属或合金储氢已取得很大进展,先后发现了Ni、Mg、Fe基三个系列的储氢材料,如图是一种储氢密度超过液氢的镍基合金的晶胞结构图.①Ni原子的基态电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2,位于周期表的d区.
②这种储氢合金的化学式为LaNi5.
分析 ①镍为28号元素,根据核外电子排布规律可以写出电子排布式,再根据元素周期表可以确定镍所在的区;
②利用均摊法可以确定化学式.
解答 解:①镍为28号元素,根据核外电子排布规律可知电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2,再根据元素周期表可以确定镍元素在d区,故答案为:1s22s22p63s23p63d84s2或[Ar]3d84s2;d;
②根据晶胞的结构图可知,在晶胞中含有La原子数为:8×$\frac{1}{8}$=1,Ni原子数为1+8×$\frac{1}{2}$=5,所以La原子数与Ni原子数之比为1:5,所以化学式为LaNi5,故答案为:LaNi5.
点评 本题主要考查了核外电子排布式和元素周期表的关系及晶体结构的掌握情况,应熟练掌握核外电子排布式和元素周期表中位置的关系.

练习册系列答案
相关题目
13. 如表为元素周期表前四周期,其中的字母代表相应的元素.
如表为元素周期表前四周期,其中的字母代表相应的元素.
(1)元素h的二价阳离子的外围电子排布式为3d6.
(2)元素c、d、e、f的第一电离能(I1)由小到大的顺序为Al<Mg<O<N.(用相应元素的元素符号表示)
(3)表中所列的元素之间可以形成多种无机化合物和有机化合物,其中1mol苯甲醛分子(如图1)中含有σ键的数目为14NA此有机物中C原子的杂化类型为sp2.
(4)元素d与e形成的化合物常用于制作耐火材料.
(5)表中有关元素形成的一种离子和单质d3互为等电子体,则该离子的化学式为NO2-.
(6)已知j的晶胞结构如图2所示,又知j的密度为9.00g/cm3,则晶胞边长为$\root{3}{\frac{4×64}{9{N}_{A}}}$cm;jkd4常作电镀液,其中kd42-的空间构型是正四面体.k原子的杂化轨道类型是sp3.
 如表为元素周期表前四周期,其中的字母代表相应的元素.
如表为元素周期表前四周期,其中的字母代表相应的元素.| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | f | g | k | ||||||||||||||
| h | I | j |
(2)元素c、d、e、f的第一电离能(I1)由小到大的顺序为Al<Mg<O<N.(用相应元素的元素符号表示)
(3)表中所列的元素之间可以形成多种无机化合物和有机化合物,其中1mol苯甲醛分子(如图1)中含有σ键的数目为14NA此有机物中C原子的杂化类型为sp2.
(4)元素d与e形成的化合物常用于制作耐火材料.
(5)表中有关元素形成的一种离子和单质d3互为等电子体,则该离子的化学式为NO2-.
(6)已知j的晶胞结构如图2所示,又知j的密度为9.00g/cm3,则晶胞边长为$\root{3}{\frac{4×64}{9{N}_{A}}}$cm;jkd4常作电镀液,其中kd42-的空间构型是正四面体.k原子的杂化轨道类型是sp3.
14.下列图中所示的实验操作评价合理的是( )
| A. | 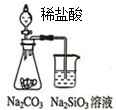 如图可能证明非金属性强弱:Cl>C>Si | |
| B. | 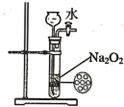 如图装置可用来制备少量氧气,并且控制反应的发生与停止 | |
| C. | 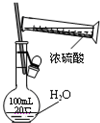 图中配制一定物质的量浓度的硫酸溶液不能直接在容量瓶中进行 | |
| D. | 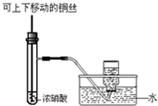 如图为制备并收集少量NO2气体 |
11.在某一电解质溶液中逐滴加入另一溶液时,溶液的导电性由大变小,至不能导电后又逐渐增大的是( )
| A. | 盐酸中逐滴加入食盐溶液 | B. | 硫酸中逐滴加入氢氧化钠溶液 | ||
| C. | 石灰乳中滴加稀盐酸 | D. | 硫酸中逐滴加入氢氧化钡溶液 |
12.甲、乙、丙、丁四种易溶水物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成.已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成.下列结论不正确的是( )
| A. | .甲溶液含有OH- | B. | .乙溶液含有H+ | C. | 丙溶液含有HCO3- | D. | .丁溶液含有NH4+ |
13.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 6.8g液态KHSO4中含有0.1NA个阳离子 | |
| B. | NA个Fe(OH)3胶体粒子形成的纳米材料的质量为107g | |
| C. | 等体积等密度的N2和CO所含分子数相同 | |
| D. | 含NA个Na+的Na2O溶解于水1L水中,Na+的物质的量浓度为1mol•L-1 |
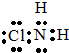 ,从物质结构的角度解释两者熔点相差较大的原因氯胺NH2Cl为分子晶体,NH4Cl为离子晶体,熔沸点离子晶体高于分子晶体.
,从物质结构的角度解释两者熔点相差较大的原因氯胺NH2Cl为分子晶体,NH4Cl为离子晶体,熔沸点离子晶体高于分子晶体.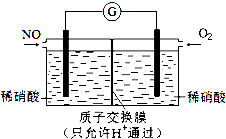 NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.
NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.