18.一定质量的C2H5OH完全燃烧时放出的热量为Q,它所生成的CO2用过量饱和石灰水完全吸收,可得200gCaCO3(相对分子质量:100)沉淀,则完全燃烧1molC2H5OH时放出的热量 ( )
| A. | Q | B. | 2Q | C. | 3Q | D. | 4Q |
17.氢气在氯气中燃烧时产生苍白色火焰.在反应过程中,破坏2mol氯气中的化学键消耗的能量为Q1kJ,破坏2mol氢气中的化学键消耗的能量为Q2kJ,形成4mol氯化氢的化学键释放的能量为Q3kJ.下列关系式中正确的是( )
| A. | Q1+Q2>Q3 | B. | Q1+Q2>2Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2=Q3 |
16.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H 2(g)+O 2(g)═2H 2O(g);△H=-483.6KJ•mol -1,则氢气的燃烧热为241.8kJ•mol -1 | |
| B. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H 2O(1);△H=-57.4kJ•mol -1则含 20.0gNaOH的稀溶液与稀醋酸完全中和,放出小于28.7kJ的热量 | |
| C. | 已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 | |
| D. | 己知2C(s)+2O 2(g)═2CO 2(g);△H=akJ•mol -1、2C(s)+O 2(g)═2CO(g);△H=bkJ•mol -1,则a>b |
11.列关于化学键的说法正确的是( )
| A. | C、N、O、H四种元素形成的化合物一定既有离子键,又有共价键 | |
| B. | 不同元素的原子构成的分子不一定只含极性共价键 | |
| C. | 含极性键的共价化合物一定是电解质 | |
| D. | HF的分子间作用力大于HCl,故HF比HCl更稳定 |
10.结合如图判断,下列叙述正确的是( )
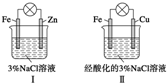

| A. | Ⅰ中不能形成原电池 | |
| B. | Ⅱ中负极反应是Fe-3e-═Fe3+ | |
| C. | Ⅱ中正极反应是O2+2H2O+4e-═4OH- | |
| D. | Ⅱ中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀 |
9.下列离子方程式的书写正确的是( )
0 151852 151860 151866 151870 151876 151878 151882 151888 151890 151896 151902 151906 151908 151912 151918 151920 151926 151930 151932 151936 151938 151942 151944 151946 151947 151948 151950 151951 151952 151954 151956 151960 151962 151966 151968 151972 151978 151980 151986 151990 151992 151996 152002 152008 152010 152016 152020 152022 152028 152032 152038 152046 203614
| A. | 过量C02通入氢氧化钙溶液中:CO2+OH-═HCO3- | |
| B. | Na202加入H2180中:2Na2O2+2H218O═4Na++4OH-+18O2↑ | |
| C. | 硅与氢氟酸的反应:Si+4H++4F-═SiF4↑+2H2↑ | |
| D. | 水玻璃中通人过量二氧化碳:Na2SiO3+CO2+H2O═2Na++CO32-+H2SiO3 |