题目内容
11.列关于化学键的说法正确的是( )| A. | C、N、O、H四种元素形成的化合物一定既有离子键,又有共价键 | |
| B. | 不同元素的原子构成的分子不一定只含极性共价键 | |
| C. | 含极性键的共价化合物一定是电解质 | |
| D. | HF的分子间作用力大于HCl,故HF比HCl更稳定 |
分析 A、C、N、O、H四种元素形成的化合物一定含有共价键,可能含有离子键;
B、不同元素的原子构成的分子可能含有非极性共价键;
C、电解质是在水溶液或熔融状态下能导电的化合物,本身能电离;
D、分子间作用力影响物质的熔沸点,与物质的稳定性无关.
解答 解:A、C、N、O、H四种元素形成的化合物一定含有共价键,可能含有离子键,如氨基酸中只含共价键,铵盐中既含共价键也含离子键,故A错误;
B、不同元素的原子构成的分子可能含有非极性共价键,如HC≡CH中含有非极性共价键,故B正确;
C、含极性键的共价化合物一定不一定是电解质,例如二氧化碳、氨气等都含极性键,但是本身都不能电离,故C错误;
D、分子间作用力影响物质的熔沸点,与物质的稳定性无关,HF共价键的键能大于HCl,所以HF比HCl更稳定,故D错误;
故选B.
点评 本题考查了化学键、分子间作用力、离子键等,侧重考查学生对概念的辨别能力,共价化合物不一定是电解质,如二氧化碳、氨气是非电解质,题目难度不大.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
2.如图所示:甲、乙之间的隔板可左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g).反应达到平衡后,恢复到反应前的温度.
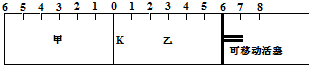
若平衡时K停留在0刻度左侧1处,则活塞停留在0刻度右侧( )

若平衡时K停留在0刻度左侧1处,则活塞停留在0刻度右侧( )
| A. | 右侧6处 | B. | 右侧6~7处 | C. | 右侧7处 | D. | 右侧7~8处 |
6.下列离子方程式中正确的是( )
| A. | H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | CH3COOH溶液与NaOH溶液反应:H++OH-═H2O | |
| C. | 铁与稀硫酸反应:Fe+2H+═Fe2++H2↑ | |
| D. | 硫酸与Cu(OH)2反应:H++OH-═H2O |
16.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H 2(g)+O 2(g)═2H 2O(g);△H=-483.6KJ•mol -1,则氢气的燃烧热为241.8kJ•mol -1 | |
| B. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H 2O(1);△H=-57.4kJ•mol -1则含 20.0gNaOH的稀溶液与稀醋酸完全中和,放出小于28.7kJ的热量 | |
| C. | 已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 | |
| D. | 己知2C(s)+2O 2(g)═2CO 2(g);△H=akJ•mol -1、2C(s)+O 2(g)═2CO(g);△H=bkJ•mol -1,则a>b |
20.下列互为同素异形体的是( )
| A. | 168O和188O | B. | CH3CH3和C6H6 | C. | 金刚石和石墨 | D. | NO和 NO2 |
1.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | 乙酸 | B. | 氨气 | C. | NH4HCO3 | D. | 氯气 |