4.关于酸和碱的下列叙述,正确的是( )
| A. | 凡是组成中含有氢元素的化合物都属于酸 | |
| B. | 凡是组成中含有OH-的化合物都属于碱 | |
| C. | 酸和碱中至少含有一种相同的元素 | |
| D. | 酸和碱中都含有金属阳离子和阴离子 |
3. 有X、Z、W三种含14个电子的粒子,其结构特点如下:
有X、Z、W三种含14个电子的粒子,其结构特点如下:
(1)X的氧化物晶体中含有化学键类型是共价键.
(2)Z与钙离子组成的化台物的电子式为Ca2+[C??C]2-.
(3)组成W的元素的简单氢化物极易溶于水的主要原因是NH3与H2O间能形成氢键,NH3与H2O都是极性分子且相互间能反应生成一水合氨,该氢化物与
空气可以构成一种燃料电池,产物为无毒物质,电解质溶液是KOH溶液,其负极的电极
反应式为2NH3-6e-+6OH-═N2+6H2O.在常温下,用该电池电解1.5L 1mol/LNaCl溶液,当消耗标准状
况下1.12LW的简单氯化物时,NaCI溶液的pH=13(假设电解过程中溶液
的体积不变).
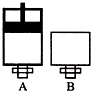
(4)M原子核外比X原予多2个电子.可逆反应2MO2(气)+O2(气)?-2MO3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,B容器可保持恒容(如图所示),若在A.、B中分别充入ImolO2和2mol MO2,使气体体积V(A)=V(B),在相同温度下反应.则:达平衡所需时间:t(A)<
t (B)(填“>”、“<”、“=”,或“无法确定”,下同).平衡时MO!的转化率:a(A)>a(B).
(5)欲比较X和M两元素的非金属性相对强弱,可采取的措施有c、d(填序号).
a.比较这两种元素的气态氢化物的沸点
b.比较这两种元素的单质在常温下的状态
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的单质与氢气化合的难易.
 有X、Z、W三种含14个电子的粒子,其结构特点如下:
有X、Z、W三种含14个电子的粒子,其结构特点如下:| 粒子代码 | X | Z | W |
| 原子核数目 | 单核 | 同种元素构成的两核 | 同种元素构成的两核 |
| 粒子的电性 | 电中性 | 两个单位负电荷 | 电中性 |
(2)Z与钙离子组成的化台物的电子式为Ca2+[C??C]2-.
(3)组成W的元素的简单氢化物极易溶于水的主要原因是NH3与H2O间能形成氢键,NH3与H2O都是极性分子且相互间能反应生成一水合氨,该氢化物与
空气可以构成一种燃料电池,产物为无毒物质,电解质溶液是KOH溶液,其负极的电极
反应式为2NH3-6e-+6OH-═N2+6H2O.在常温下,用该电池电解1.5L 1mol/LNaCl溶液,当消耗标准状
况下1.12LW的简单氯化物时,NaCI溶液的pH=13(假设电解过程中溶液
的体积不变).
(4)M原子核外比X原予多2个电子.可逆反应2MO2(气)+O2(气)?-2MO3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,B容器可保持恒容(如图所示),若在A.、B中分别充入ImolO2和2mol MO2,使气体体积V(A)=V(B),在相同温度下反应.则:达平衡所需时间:t(A)<
t (B)(填“>”、“<”、“=”,或“无法确定”,下同).平衡时MO!的转化率:a(A)>a(B).
(5)欲比较X和M两元素的非金属性相对强弱,可采取的措施有c、d(填序号).
a.比较这两种元素的气态氢化物的沸点
b.比较这两种元素的单质在常温下的状态
c.比较这两种元素的气态氢化物的稳定性
d.比较这两种元素的单质与氢气化合的难易.
2.钯的化合物氯化钯可用来检测有毒气体CO,常温发生反应的化学方程式为:CO+PdCl2+H2O═CO2+Pd↓+2HC1,下列说法正确的是( )
| A. | 氧化性:PdCl2>CO2 | |
| B. | 生成22.4LCO2时,转移的电子为2mo1 | |
| C. | 反应中PdCl2被氧化 | |
| D. | CO气体只有在高温下才能表现还原性 |
1.实验室制Cl2的反应如下:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,下列有关该反应的说法正确的是( )
| A. | MnO2是还原剂 | B. | HCl被氧化 | ||
| C. | MnO2发生氧化反应 | D. | 每反应4molHCl转移4mol电子 |
20.下列有关物质的性质及应用说法正确的是( )
| A. | 石英坩埚耐高温,可用来加热熔融氢氧化钠固体 | |
| B. | 聚氯乙烯塑料在日常生活中可用来进行食品包装 | |
| C. | 硫酸亚铁溶液和水玻璃在空气中久置后均变质 | |
| D. | 甲醛可用作食品防腐剂 |
19.常温时,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
| A. | 某HCl溶液的pH值为2,则溶液中由水电离的c(H+)=10-2mol•L-1 | |
| B. | 0.1 mol•L-1的KHA溶液,其pH=10,c(K+)>c(A2-)>c(HA-)>c(OH-) | |
| C. | 等体积、等物质的量浓度的Na2CO3溶液与NaHCO3溶液混合:3c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) | |
| D. | 将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1NaOH溶液等体积混合后溶液pH>7,则反应后的混合液:c(HA)>C(Na+)>c(A-) |
18.下列反应的离子方程式书写正确的是( )
| A. | Na2O溶于水:Na2O+H2O=2Na++2OH- | |
| B. | 向Ca(ClO)2溶液中通入过量CO2:2ClO-+H2O+CO2=2HClO+CO32- | |
| C. | 用FeCl3溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+ | |
| D. | 碳酸钙溶于稀醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
17.设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 常温常压下,1.7gNH3所含的电子数为0.8NA | |
| B. | 标准状况下,11.2LSO3所含的氧原子数为1.5NA | |
| C. | 1molSiO2中含有Si-O键的数目为2NA | |
| D. | 1molFe与足量的稀硝酸反应,转移的电子总数为3NA |
15.某不纯的烧碱样品中各成分的质量分数如表所示:
取a g样品溶于50mL2mol/L的盐酸中,充分反应后,再用适量2mol/LNaOH溶液将剩余的酸恰好中和,最后将溶液蒸干,可得干燥固体的质量为( )
0 151801 151809 151815 151819 151825 151827 151831 151837 151839 151845 151851 151855 151857 151861 151867 151869 151875 151879 151881 151885 151887 151891 151893 151895 151896 151897 151899 151900 151901 151903 151905 151909 151911 151915 151917 151921 151927 151929 151935 151939 151941 151945 151951 151957 151959 151965 151969 151971 151977 151981 151987 151995 203614
| 成分 | NaOH | Na2CO3 | H2O |
| 质量分数 | 90.4% | 3.8% | 5.8% |
| A. | 2.34 g | B. | 4.68 g | C. | 5.85 g | D. | (2.34-a) g |
 ,若该反应生成标况下氢气11.2L,则此时反应转移的电子数目是0.5NA.
,若该反应生成标况下氢气11.2L,则此时反应转移的电子数目是0.5NA.