��Ŀ����
3��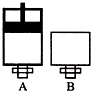 ��X��Z��W���ֺ�14�����ӵ����ӣ���ṹ�ص����£�
��X��Z��W���ֺ�14�����ӵ����ӣ���ṹ�ص����£�| ���Ӵ��� | X | Z | W |
| ԭ�Ӻ���Ŀ | ���� | ͬ��Ԫ�ع��ɵ����� | ͬ��Ԫ�ع��ɵ����� |
| ���ӵĵ��� | ������ | ������λ����� | ������ |
��2��Z���������ɵĻ�̨��ĵ���ʽΪCa2+[C??C]2-��
��3�����W��Ԫ�صļ��⻯�K������ˮ����Ҫԭ����NH3��H2O�����γ������NH3��H2O���Ǽ��Է���������ܷ�Ӧ����һˮ�ϰ������⻯����
�������Թ���һ��ȼ�ϵ�أ�����Ϊ�����ʣ��������Һ��KOH��Һ���为���ĵ缫
��ӦʽΪ2NH3-6e-+6OH-�TN2+6H2O���ڳ����£��øõ�ص��1.5L 1mol/LNaCl��Һ�������ı�״
����1.12LW�ļ��Ȼ���ʱ��NaCI��Һ��pH=13���������������Һ
��������䣩��
��4��Mԭ�Ӻ����Xԭ���2�����ӣ����淴Ӧ2MO2������+O2������?-2MO3�������������ܱ������н��У�A��������һ���������ƶ��Ļ�����B�����ɱ��ֺ��ݣ���ͼ��ʾ��������A����B�зֱ����ImolO2��2mol MO2��ʹ�������V��A��=V��B��������ͬ�¶��·�Ӧ����ƽ������ʱ�䣺t��A����
t ��B���������������������=��������ȷ��������ͬ����ƽ��ʱMO!��ת���ʣ�a��A����a��B����
��5�����Ƚ�X��M��Ԫ�صķǽ��������ǿ�����ɲ�ȡ�Ĵ�ʩ��c��d������ţ���
a���Ƚ�������Ԫ�ص���̬�⻯��ķе�
b���Ƚ�������Ԫ�صĵ����ڳ����µ�״̬
c���Ƚ�������Ԫ�ص���̬�⻯����ȶ���
d���Ƚ�������Ԫ�صĵ������������ϵ����ף�
���� X��Z��W���ֺ�14�����ӵ����ӣ�XΪ���ˣ������ԣ���X��������Ϊ14��XΪSiԭ�ӣ�ZΪͬԪ�ع��ɵ��������ӣ�������λ����ɣ����γ�ZԪ�ص�ԭ��������Ϊ$\frac{14-2}{2}$=6����ZΪC22-��WΪͬԪ�ع��ɵ��������ӣ������ԣ����γ�WԪ�ص�ԭ��������Ϊ$\frac{14}{2}$=7��ΪNԪ�أ�WΪN2��Mԭ�Ӻ����Xԭ���2�����ӣ���MΪS���ݴ˴��⣮
��� �⣺X��Z��W���ֺ�14�����ӵ����ӣ�XΪ���ˣ������ԣ���X��������Ϊ14��XΪSiԭ�ӣ�ZΪͬԪ�ع��ɵ��������ӣ�������λ����ɣ����γ�ZԪ�ص�ԭ��������Ϊ$\frac{14-2}{2}$=6����ZΪC22-��WΪͬԪ�ع��ɵ��������ӣ������ԣ����γ�WԪ�ص�ԭ��������Ϊ$\frac{14}{2}$=7��ΪNԪ�أ�WΪN2��Mԭ�Ӻ����Xԭ���2�����ӣ���MΪS��
��1��X��������Ϊ�������裬�������辧���к��л�ѧ�������ǹ��ۼ���
�ʴ�Ϊ�����ۼ���
��2��ZΪC22-��Z���������ɵĻ�̨��ĵ���ʽΪ Ca2+[C??C]2-��
�ʴ�Ϊ��Ca2+[C??C]2-��
��3��WΪN2�����W��Ԫ�صļ��⻯��Ϊ������NH3��H2O�����γ������NH3��H2O���Ǽ��Է���������ܷ�Ӧ����һˮ�ϰ�����������������ˮ��������������Թ���һ��ȼ�ϵ�أ�����Ϊ������ӦΪ������ˮ���������Һ��KOH��Һ���õ���а����ǻ�ԭ�����ڸ�������������Ӧ���缫��ӦʽΪ 2NH3-6e-+6OH-�TN2+6H2O�����ݵ缫��Ӧʽ��֪�����ı�״����1.12L��0.05mol����ʱ��ת�Ƶ��ӵ����ʵ���Ϊ0.15mol�����1.5L 1mol/LNaCl��Һ������0.15mol�������ƣ���Һ����������Ũ��Ϊ$\frac{0.15mol}{1.5L}$=0.1mol/L��������Һ��pH=13��
�ʴ�Ϊ��NH3��H2O�����γ������NH3��H2O���Ǽ��Է���������ܷ�Ӧ����һˮ�ϰ���2NH3-6e-+6OH-�TN2+6H2O��13��
��4�����淴Ӧ2SO2������+O2������?2SO3�������������ܱ������н��У�A��������һ���������ƶ��Ļ�����B�����ɱ��ֺ��ݣ�����A��B�зֱ����1molO2��2mol SO2��ʹ�������V��A��=V��B��������ͬ�¶��·�Ӧ�����ڸ÷�ӦΪ���������С�ķ�Ӧ������A�����е�ѹǿ����B����������t��A��t����B��ƽ��ʱSO2��ת���ʣ�a��A����a��B����
�ʴ�Ϊ����������
��5���Ƚ�Si��S��Ԫ�صķǽ��������ǿ�������Ը�����̬�⻯����ȶ��ԡ��������������ϵ��������жϣ������ܸ�����̬�⻯��ķе㼰�����ڳ����µ�״̬�жϣ���ѡc��d��
���� ���⿼��Ԫ�ػ������ƶϡ����û�ѧ����缫��Ӧ��Ӱ�컯ѧƽ���ƶ������ء�Ԫ�������ɵȣ��Ѷ��еȣ�ע�����֪ʶ��������ã�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | �ܣ��ۣ��ڣ��� | B�� | �ۣ��ܣ��ڣ��� | C�� | �ڣ��ۣ��ܣ��� | D�� | �ۣ��ڣ��ܣ��� |
| A�� | Na2O����ˮ��Na2O+H2O=2Na++2OH- | |
| B�� | ��Ca��ClO��2��Һ��ͨ�����CO2��2ClO-+H2O+CO2=2HClO+CO32- | |
| C�� | ��FeCl3��Һ��ʴͭ�壺Fe3++Cu=Fe2++Cu2+ | |
| D�� | ̼�������ϡ���CaCO3+2H+=Ca2++CO2��+H2O |
| A�� |  | B�� | C3H6 | C�� |  | D�� | CH2CHCH3 |
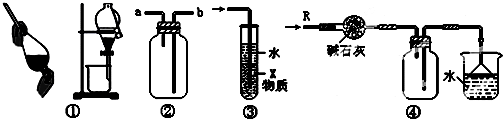
| A�� | װ�âٿ����ڷ����Ҵ���ˮ�Ļ���� | |
| B�� | װ�âڿ������ռ�H2��NH3��CO2��Cl2��HCl��NO2������ | |
| C�� | װ�â���X��Ϊ���Ȼ�̼�����������հ������Ȼ��⣬����ֹ���� | |
| D�� | װ�âܿ����ڸ���ռ������������ն���İ��� |
| A�� | ��ơ��ƿ�ǣ������������� | |
| B�� | ϡ��CH3COOHʱ����Һ��CH3COO-��Ŀ���� | |
| C�� | ��ҵ�ϳɰ�����500�����ҵ��¶� | |
| D�� | �ȵĴ�����Һ��ȥ��Ч������ĺ� |
| A�� | NA���κ����������ռ�����Լ��22.4L | |
| B�� | NA��H3O+���е�����ĿΪ11NA | |
| C�� | 0.5mol/L NaOH��Һ�к���0.5NA��Na+ | |
| D�� | NA��CO2��NO2�Ļ����������ԭ����ĿΪ2NA |