某无色溶液中只可能含有Na+、Ba2+、Cl-、Br-、SO 、SO
、SO ,对该溶液进行下列实验,实验操作和现象如下表:
,对该溶液进行下列实验,实验操作和现象如下表:
| 步骤 | 操作 | 现象 |
| (1) | 取少量溶液滴加几滴石蕊试液 | 溶液变蓝 |
| (2) | 另取少量溶液滴加过量氯水,再加入CCl4溶液,振荡,静置 | 上层无色,下层呈橙红色 |
| (3) | 取(2)上层溶液,加入过量Ba(NO3)2溶液和稀HNO3,过滤 | 有白色沉淀产生 |
| (4) | 向(3)的滤液中加入过量AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
下列结论正确的是( )
A.可能含有Cl-、SO 、SO
、SO B.肯定没有Ba2+、Cl-、Br-
B.肯定没有Ba2+、Cl-、Br-
C.不能确定Na+、SO 、SO
、SO D.肯定含有Na+、Br-、SO
D.肯定含有Na+、Br-、SO
部分中学化学常见元素原子结构及性质如下表所示:
| 元素 | 结构及性质 |
| A | A单质是生活中的常见金属,它有两种氯化物,相对分子质量相差35.5 |
| B | B原子最外层电子数是内层电子总数的1/5 |
| C | C是常见化肥的主要元素,单质常温下呈气态 |
| D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| E | 通常情况下,E没有最高正化合价,其单质之一是空气的一种主要成分 |
| F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(1)A元素在周期表中的位置为______________。
(2)B与C形成的化合物的化学式为________,它属于________(填“离子”或“共价”)化合物。
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是____________________________;
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显______性,N的结构式为______________________。
(4)B~F各元素原子半径由小到大的顺序是__________(用元素符号表示)。
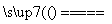 8Cu+4FeO+2Fe2O3+16SO2↑,若CuFeS2中铁元素为+2价,则反应中被还原的元素为________(填元素名称)。
8Cu+4FeO+2Fe2O3+16SO2↑,若CuFeS2中铁元素为+2价,则反应中被还原的元素为________(填元素名称)。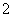 、Cl-的转化率与溶液的pH的关系如图所示。则pH=8时,ClO2被还原为________。
、Cl-的转化率与溶液的pH的关系如图所示。则pH=8时,ClO2被还原为________。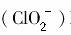 对人体不利。欲在弱碱性条件下将水中的
对人体不利。欲在弱碱性条件下将水中的
 (2)整个过程中的还原剂是________。
(2)整个过程中的还原剂是________。 氧化成NO
氧化成NO ,如果不考虑过程中硝化细菌的增殖,其反应如下所示:
,如果不考虑过程中硝化细菌的增殖,其反应如下所示: 请完成上述离子方程式的配平。
请完成上述离子方程式的配平。