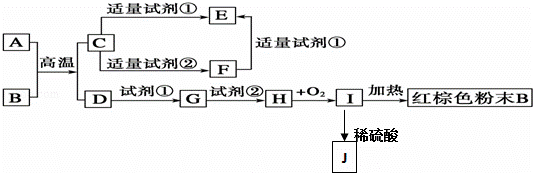
氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等.为获得纯净的氧化铜,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
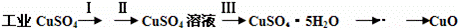
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
(1)步骤Ⅰ的目的是除不溶性杂质.所需操作的名称是 溶解、过滤 .
(2)步骤Ⅱ的目的是除硫酸亚铁.操作步骤是先滴加H2O2溶液,稍加热,当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以调整溶液pH在一定范围之内,加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1.
①写出用H2O2溶液除去硫酸亚铁的离子方程式 .
②调整pH 的范围应该在 之间.
(3)步骤Ⅲ的目的是得到CuSO4•5H2O晶体.操作是将溶液加热蒸发至有晶膜出现时,停止加热, ,水浴加热烘干.采用水浴加热的原因是 .
(4)该同学用CuSO4溶液进行如下探究实验:
取A、B两支试管,分别加入 2mL 5% H2O2溶液,再向H2O2溶液中分别滴入0.1mol•L﹣1FeCl3和CuSO4 溶液各1mL,摇匀,观察到滴入FeCl3 溶液的试管产生气泡更快,由此得到结论:Fe3+对H2O2溶液分解的催化效率比Cu2+高,该同学的结论是否正确 (填正确或错误),请说明原因 .
X、Y、Z、W是短周期的4种元素,有关他们的信息如下表所示.
| 元素 | 部分结构知识 | 部分性质 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n﹣3(n为原子核外电子层数) | 化学反应中,W原子易失去最外层电子形成与Ne原子电子层结构相同的Wn+ |
填写下列空白(提示:不能用字母X、Y、Z、W作答):
(1)X的气态氢化物分子的结构式是 ,Z元素在周期表中的位置是 .
(2)X、Y、Z三元素的最高价氧化物对应的水化物酸性由强到弱的顺序是 .
(3)常温时,W的硫酸盐溶液的pH 7(填“=”“>”或“<”).理由是 (用离子方程式表示).
(4)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是 (用离子方程式表示).
(5)W与氧化铁反应的化学方程式 .
将一定量的锌与100mL 18.5mol•L﹣1浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6L(标准状况).将反应后的溶液稀释至1L,则得溶液中c(H+)=0.1mol•L﹣1,则下列叙述中错误的是( )
|
| A. | 气体A为SO2和H2的混合物 | B. | 气体A中SO2和H2的体积比为1:5 |
|
| C. | 反应中消耗的Zn的质量为97.5 g | D. | 反应中共转移电子3 mol |
某同学设计了以下流程来检验碳酸钾粉末中含有少量氯化钾和氢氧化钾.下列说法不正确的是( )

|
| A. | 步骤3的操作名称是过滤 |
|
| B. | 步骤1所需玻璃仪器是烧杯和玻璃棒 |
|
| C. | 试剂A是BaCl2溶液 |
|
| D. | 加入试剂A 的目的是除去CO32﹣并避免对Cl﹣或OH﹣的检验的干扰 |
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素( )
|
| A. | 在自然界中只以化合态的形式存在 | B. | 单质常用作半导体材料和光导纤维 |
|
| C. | 最高价氧化物不与酸反应 | D. | 气态氢化物比甲烷稳定 |
观察是研究物质性质的一种基本方法.一同学将一小块金属钠露置于空气中,观察到下列现象:银白色 变灰暗
变灰暗 变白色
变白色 出现液滴
出现液滴 白色固体,下列说法正确的是( )
白色固体,下列说法正确的是( )
|
| A. | ①发生了氧化还原反应 |
|
| B. | ②变白色是因为生成了碳酸钠 |
|
| C. | ③是碳酸钠吸收空气中的水蒸气形成了溶液 |
|
| D. | ④只发生物理变化 |
用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:下列叙述正确的是( )

|
| A. | 试剂X可以是盐酸 |
|
| B. | 反应①过滤后所得沉淀为氢氧化铁 |
|
| C. | 图中所示转化反应都不是氧化还原反应 |
|
| D. | 操作②中发生的化学方程式为NaAlO2+2H2O+CO2=Al(OH)3↓+NaHCO3 |
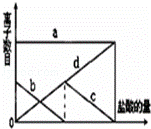
少量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化.四条曲线(c和d图象部分重叠)溶液中离子的对应关系,正确的是( )
|
| A. | a:Cl﹣b:K+ c:CO32﹣ d:HCO3﹣ |
|
| B. | a:K+ b:CO32﹣ c:Cl﹣ d:HCO3﹣ |
|
| C. | a:K+ b:CO32﹣ c:HCO3﹣ d:Cl﹣ |
|
| D. | a:K+b:HCO3﹣ c:Cl﹣ d:CO32﹣ |
某氧化物不溶于水,溶于熔化的NaOH中,生成易溶于水的化合物,向稀盐酸中滴加所生成化合物的水溶液,立即有白色沉淀产生,则原氧化物是( )
|
| A. | Al2O3 | B. | MgO | C. | SiO2 | D. | P2O5 |