0 135450 135458 135464 135468 135474 135476 135480 135486 135488 135494 135500 135504 135506 135510 135516 135518 135524 135528 135530 135534 135536 135540 135542 135544 135545 135546 135548 135549 135550 135552 135554 135558 135560 135564 135566 135570 135576 135578 135584 135588 135590 135594 135600 135606 135608 135614 135618 135620 135626 135630 135636 135644 203614
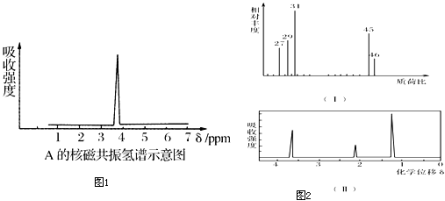
 ,某有机物X的键线式为:
,某有机物X的键线式为:
 肼(N2H4)是一种高能燃料,在工业生产中用途广泛.
肼(N2H4)是一种高能燃料,在工业生产中用途广泛.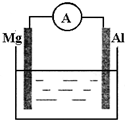 如图所示装置:
如图所示装置: (g)→
(g)→ (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol;
 用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:
用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下: