0 133726 133734 133740 133744 133750 133752 133756 133762 133764 133770 133776 133780 133782 133786 133792 133794 133800 133804 133806 133810 133812 133816 133818 133820 133821 133822 133824 133825 133826 133828 133830 133834 133836 133840 133842 133846 133852 133854 133860 133864 133866 133870 133876 133882 133884 133890 133894 133896 133902 133906 133912 133920 203614
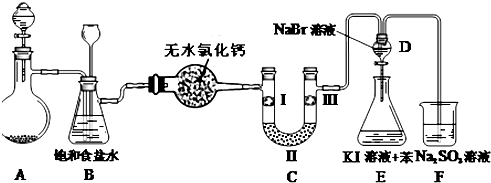
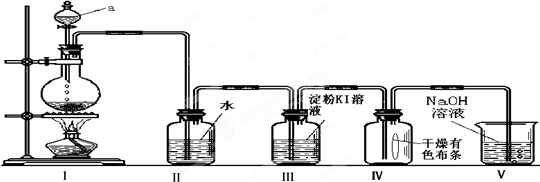
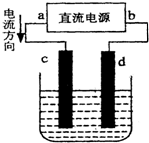
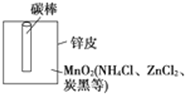 某学校设计了一节实验活动课,让学生从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质.整个实验过程如下,请回答有关问题:
某学校设计了一节实验活动课,让学生从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质.整个实验过程如下,请回答有关问题: (Ⅰ)2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.请回答下列问题:
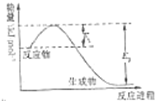
(Ⅰ)2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.请回答下列问题:
 氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题:
氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题: