题目内容
 某学校设计了一节实验活动课,让学生从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质.整个实验过程如下,请回答有关问题:
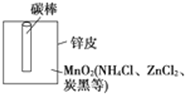
某学校设计了一节实验活动课,让学生从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质.整个实验过程如下,请回答有关问题:(1)干电池的基本构造和工作原理.如图为干电池的基本构造图.干电池工作时负极上的电极反应式是
(2)锌皮和碳棒的回收.用钳子和剪刀剪开回收的干电池的锌铜,将锌皮和碳棒取出,并用毛刷刷干净,将电池内的黑色粉末移入小烧杯中.
(3)氯化铵、氯化锌的提取、检验和分离.
①如何从黑色粉末中提取NH4Cl和ZnCl2等晶体的混合物?写出简要的实验步骤:
②设计简单的实验证明所得晶体中含有NH4+
实验步骤:
实验现象:
有关的离子方程式:
③用什么方法可将NH4Cl和ZnCl2的晶体混合物分离开?
考点:物质分离和提纯的方法和基本操作综合应用,原电池和电解池的工作原理,物质的检验和鉴别的实验方案设计
专题:实验设计题,电化学专题
分析:(1)负极为锌,被氧化生成锌离子;正极上NH4+得电子被还原生成氨气;
(3)①根据不溶物以及NH4Cl和ZnCl2的性质选择分离的方法,不溶物质可直接过滤,用结晶的方法分离NH4Cl和ZnCl2;
②将晶体溶于水,加入氢氧化钠,并加热,生成的气体用湿润的红色石蕊试纸检验;
③根据NH4Cl易分解的性质选取分离方法.
(3)①根据不溶物以及NH4Cl和ZnCl2的性质选择分离的方法,不溶物质可直接过滤,用结晶的方法分离NH4Cl和ZnCl2;
②将晶体溶于水,加入氢氧化钠,并加热,生成的气体用湿润的红色石蕊试纸检验;
③根据NH4Cl易分解的性质选取分离方法.
解答:
解:(1)在锌锰干电池中,活泼金属锌为电池负极,反应式为Zn-2e-=Zn2+,正极上NH4+得电子被还原生成氨气,电极方程式为2NH4++2e-=2NH3↑+H2↑,
故答案为:Zn-2e-=Zn2+;2NH4++2e-=2NH3↑+H2↑;
(3)①黑色粉末既有可溶性的NH4Cl和ZnCl2,又有不溶物,所以可以采用溶解、过滤、结晶的办法得到ZnCl2和NH4Cl的混合物,具体操作为向小烧杯中加入一定量的蒸馏水,充分搅拌,然后过滤,将滤液移入蒸发皿中,加热蒸发结晶,
故答案为:向小烧杯中加入一定量的蒸馏水,充分搅拌,然后过滤,将滤液移入蒸发皿中,加热蒸发结晶;
②实验证明所得晶体中含有NH4+,可取少量晶体溶于蒸馏水配成溶液.取少许溶液,加入少量NaOH溶液后加热,将湿润的红石蕊试纸放在试管口,如观察到试纸变蓝,可说明存在NH4+,反应的离子方程式为NH4++OH-
NH3↑+H2O,
故答案为:取少量晶体溶于蒸馏水配成溶液.取少许溶液,加入少量NaOH溶液后加热,将湿润的红石蕊试纸放在试管口;
实验现象:试纸变蓝;
有关离子方程式:NH4++OH-
NH3↑+H2O;
③NH4Cl具有热不稳定性,而且稳定性降低时又能马上化合生成氯化铵,因此可以采用加热方法,故答案为:加热.
故答案为:Zn-2e-=Zn2+;2NH4++2e-=2NH3↑+H2↑;
(3)①黑色粉末既有可溶性的NH4Cl和ZnCl2,又有不溶物,所以可以采用溶解、过滤、结晶的办法得到ZnCl2和NH4Cl的混合物,具体操作为向小烧杯中加入一定量的蒸馏水,充分搅拌,然后过滤,将滤液移入蒸发皿中,加热蒸发结晶,
故答案为:向小烧杯中加入一定量的蒸馏水,充分搅拌,然后过滤,将滤液移入蒸发皿中,加热蒸发结晶;
②实验证明所得晶体中含有NH4+,可取少量晶体溶于蒸馏水配成溶液.取少许溶液,加入少量NaOH溶液后加热,将湿润的红石蕊试纸放在试管口,如观察到试纸变蓝,可说明存在NH4+,反应的离子方程式为NH4++OH-
| ||
故答案为:取少量晶体溶于蒸馏水配成溶液.取少许溶液,加入少量NaOH溶液后加热,将湿润的红石蕊试纸放在试管口;
实验现象:试纸变蓝;
有关离子方程式:NH4++OH-
| ||
③NH4Cl具有热不稳定性,而且稳定性降低时又能马上化合生成氯化铵,因此可以采用加热方法,故答案为:加热.
点评:本题是以实验为主的综合题,考查物质的提取、分离、检验及电化学知识,题目较为综合,具有一定难度,学习中注意化学实验知识的积累.

练习册系列答案
相关题目
在0.25mol H2O中,含有的氧原子数约为( )
| A、1个 |
| B、0.25个 |
| C、1.5×1023个 |
| D、6.02×1023个 |
常温下,某溶液中由水电离产生的c(H+)等于10-11mol?L-1,则该溶液的pH可能是( )
| A、3 | B、7 | C、8 | D、12 |
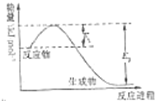 氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题:
氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题: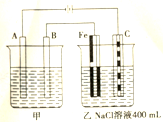 下图为相互串联的甲乙两个电解池,试回答:
下图为相互串联的甲乙两个电解池,试回答: