题目内容
250mL的盐酸和足量的锌反应,放出氢气11.2L(标况下),求:
(1)盐酸的物质的量浓度是多少?
(2)消耗锌的质量为多少克?
(1)盐酸的物质的量浓度是多少?
(2)消耗锌的质量为多少克?
考点:化学方程式的有关计算
专题:计算题
分析:根据V=nVm计算氢气的n(H2),根据方程式Zn+2HCl=ZnCl2+H2↑,计算HCl的物质的量,再根据c=
计算盐酸的物质的量浓度;代入m=nM计算质量.
| n |
| V |
解答:
解:n(H2)=
=0.05mol,
Zn+2HCl=ZnCl2+H2↑,
65g 2mol 1mol
m n 0.05mol
m=
=3.25g,
n(HCl)=
=0.1mol,
c(HCl)=
=0.4mol/L,
答:参加反应的锌的质量是3.25g,所用盐酸中HCl的物质的量浓度为0.4mol/L.
| 11.2L |
| 22.4L/mol |
Zn+2HCl=ZnCl2+H2↑,
65g 2mol 1mol
m n 0.05mol
m=
| 65g×0.05mol |
| 1mol |
n(HCl)=
| 2mol×0.05mol |
| 1mol |
c(HCl)=
| 0.1mol |
| 0.25L |
答:参加反应的锌的质量是3.25g,所用盐酸中HCl的物质的量浓度为0.4mol/L.
点评:本题考查根据方程式的计算、常用化学计量的有关计算,比较基础,注意基础知识的理解掌握.

练习册系列答案
相关题目
0.2mol有机物和0.4mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g).产物经过浓硫酸后,浓硫酸的质量增加10.8g;再通过灼热CuO充分反应后,固体质量减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g.0.1mol该有机物恰好与4.6g金属钠完全反应.下列关于该有机物的说法不正确的是( )
| A、该化合物的相对分子质量是62 |
| B、该化合物的化学式为C2H6O2 |
| C、1 mol该化合物能与2 mol O2发生催化氧化反应 |
| D、1 mol该有机物最多能与2 mol Na反应 |
下列说法正确的是( )
| A、实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| B、用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度 |
| C、石油的分馏是物理变化,而煤的干馏是化学变化 |
| D、将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
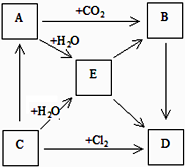 如图表示A、B、C、D、E五种物质的相互转化关系,其中A为淡黄色固体,C为金属单质,D为最常用的调味品.
如图表示A、B、C、D、E五种物质的相互转化关系,其中A为淡黄色固体,C为金属单质,D为最常用的调味品.
 (1)铁、铝、铜是人类使用广泛的三种金属.
(1)铁、铝、铜是人类使用广泛的三种金属.