0 133300 133308 133314 133318 133324 133326 133330 133336 133338 133344 133350 133354 133356 133360 133366 133368 133374 133378 133380 133384 133386 133390 133392 133394 133395 133396 133398 133399 133400 133402 133404 133408 133410 133414 133416 133420 133426 133428 133434 133438 133440 133444 133450 133456 133458 133464 133468 133470 133476 133480 133486 133494 203614
 下面是用10mol/L的浓H2SO4配制成浓度为0.1mol/L的 500mL稀H2SO4的操作,请按要求填空:
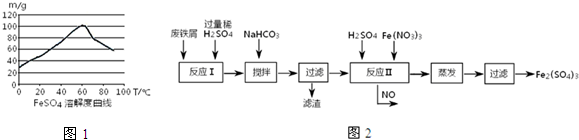
下面是用10mol/L的浓H2SO4配制成浓度为0.1mol/L的 500mL稀H2SO4的操作,请按要求填空: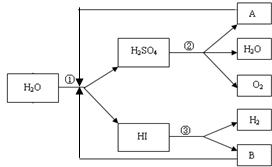 人类研究氢能源从未间断过,而热化学循环分解水制氢气是在水反应体系中加入一种中间物,经历不同的反应阶段,最终将水分解为氢气和氧气,这是一种节约能源、节省反应物料的技术,如图是一个热化学循环制氢气法的流程:
人类研究氢能源从未间断过,而热化学循环分解水制氢气是在水反应体系中加入一种中间物,经历不同的反应阶段,最终将水分解为氢气和氧气,这是一种节约能源、节省反应物料的技术,如图是一个热化学循环制氢气法的流程: