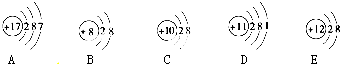题目内容
 下面是用10mol/L的浓H2SO4配制成浓度为0.1mol/L的 500mL稀H2SO4的操作,请按要求填空:
下面是用10mol/L的浓H2SO4配制成浓度为0.1mol/L的 500mL稀H2SO4的操作,请按要求填空:(1)配制过程中所需要的玻璃仪器主要有:量筒、烧杯、玻璃棒、
(2)所需浓H2SO4的体积为
(3)将量取的浓H2SO4沿器皿内壁慢慢注入盛有约100mL水的
(4)待溶液恢复到室温后,将上述溶液沿玻璃棒注入容量瓶中,并用50mL蒸馏水洗涤烧杯2~3次,洗涤液要容量瓶中,并摇匀.
(5)加水至距刻度线1-2cm,改用
(6)倒转摇匀
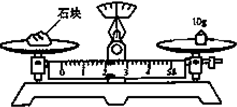
(7)某同学用托盘天平称量的某石块的质量,读数如图所示,其读数的准确值是
考点:溶液的配制
专题:实验题
分析:(1)根据配制一定物质的量浓度的溶液的步骤选择使用的仪器;
(2)根据溶液的稀释过程中溶质的物质的量不变计算出需要浓硫酸的体积;根据浓硫酸的体积选择量筒规格;
(3)溶液的稀释一般在烧杯里进行;
(5)定容时,开始时可以直接将蒸馏水倒入容量瓶,在距刻度线1-2cm时,要改用胶头滴管逐滴滴加;
(7)根据m物=m砝+m游来计算.
(2)根据溶液的稀释过程中溶质的物质的量不变计算出需要浓硫酸的体积;根据浓硫酸的体积选择量筒规格;
(3)溶液的稀释一般在烧杯里进行;
(5)定容时,开始时可以直接将蒸馏水倒入容量瓶,在距刻度线1-2cm时,要改用胶头滴管逐滴滴加;
(7)根据m物=m砝+m游来计算.
解答:
解:(1)配制0.1mol/L的稀H2SO4 500mL的步骤有:计算、量取、稀释、冷却、转移、洗涤、定容、摇匀等,需要的玻璃仪器有:量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以还需要的仪器为:500mL容量瓶、胶头滴管,
故答案为:500mL容量瓶;胶头滴管;
(2)设所需浓H2SO4的体积为Vml,根据溶液的稀释过程中溶质的物质的量不变可知:10mol/L×Vml×10-3=0.1mol/L×0.5L
解得V=5.0ml,故应选用10ml的量筒.故答案为:5.0;10;
(3)溶液的稀释一般在烧杯里进行,故答案为:烧杯;
(5)定容时,开始时可以直接将蒸馏水倒入容量瓶,在距刻度线1-2cm时,要改用胶头滴管逐滴滴加,故答案为:胶头滴管;
(7)从图象可知,m砝=10g,m游=2.1g,根据m物=m砝+m游可知,石块的质量m=10g+2.1g=12.1g,故答案为:12.1.
故答案为:500mL容量瓶;胶头滴管;
(2)设所需浓H2SO4的体积为Vml,根据溶液的稀释过程中溶质的物质的量不变可知:10mol/L×Vml×10-3=0.1mol/L×0.5L
解得V=5.0ml,故应选用10ml的量筒.故答案为:5.0;10;
(3)溶液的稀释一般在烧杯里进行,故答案为:烧杯;
(5)定容时,开始时可以直接将蒸馏水倒入容量瓶,在距刻度线1-2cm时,要改用胶头滴管逐滴滴加,故答案为:胶头滴管;
(7)从图象可知,m砝=10g,m游=2.1g,根据m物=m砝+m游可知,石块的质量m=10g+2.1g=12.1g,故答案为:12.1.
点评:本题考查了一定物质的量浓度溶液的配制过程中的计算、仪器的选择和使用以及具体的操作,考查的内容很基础,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
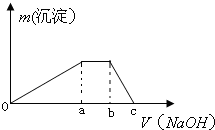 甲是一种盐,由A、B、C、D、E五种短周期元素元素组成.甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子.A元素原子核内质子数比E的少1,D、E处于同主族.用甲进行如下实验:
甲是一种盐,由A、B、C、D、E五种短周期元素元素组成.甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子.A元素原子核内质子数比E的少1,D、E处于同主族.用甲进行如下实验: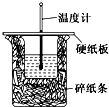 50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: