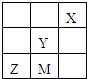
 四种非金属主族元素M、X、Y、Z在周期表中相对位置如图,下列判断不正确的是( )
四种非金属主族元素M、X、Y、Z在周期表中相对位置如图,下列判断不正确的是( )| A、Z的氢化物中中心原子的杂化方式为sp3 |
| B、Z原子的第一电离能小于M原子的第一电离能 |
| C、四种元素全部位于p区 |
| D、M、Y、Z最高价氧化物对应水化物的酸性从强到弱的顺序为:Y>M>Z |
下列物质中,属于原子晶体的化合物是( )
| A、水晶 | B、晶体硅 |
| C、金刚石 | D、干冰 |
在2molNa2SO4中,含有Na+的数目是( )
| A、1.204×1024 |
| B、1.204×1023 |
| C、2.408×1024 |
| D、2.408×1023 |
下列有机物命名正确的是( )
A、1,3,4-三甲苯 |
B、α-氨基苯丙酸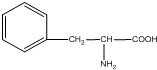 |
| C、2-甲基丙烯 (CH3)2C=CH2 |
| D、2,2-二甲基-3-丁醇 (CH3)3C-CHOH-CH3 |
为证明某可溶性一元酸(HX)是弱酸,某同学设计了如下实验方案,其中不 合理的是( )
| A、室温下,测0.1 mol/L HX溶液的pH>1,证明HX是弱酸 |
| B、室温下,将等浓度等体积的盐酸和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 |
| C、室温下,测1 mol/L NaX的pH,若pH>7,证明HX是弱酸 |
| D、在相同条件下,对0.1 mol/L的盐酸和0.1 mol/L的HX溶液进行导电性实验,若HX溶液灯泡较暗,证明HX为弱酸 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、78 g Na2O2与足量水反应中电子转移了0.2NA |
| B、1 mol甲基中含有7 NA 个电子 |
| C、62 g白磷中含P-P键为3 NA |
| D、1 mol氖气含有的原子数为2 NA |
以氯乙烷为原料制取乙二酸(HOOC-COOH)过程中,要依次经过下列步骤中的( )
①与NaOH的水溶液共热
②与NaOH的醇溶液共热
③与浓硫酸共热到170℃
④在一定条件下与氯气加成
⑤在催化剂存在的情况下与氧气共热.
①与NaOH的水溶液共热
②与NaOH的醇溶液共热
③与浓硫酸共热到170℃
④在一定条件下与氯气加成
⑤在催化剂存在的情况下与氧气共热.
| A、①③④①⑤ | B、②④①⑤ |
| C、①③④② | D、③④①⑤ |
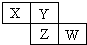 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )| A、氢化物的稳定性:X>Y |
| B、W的最高价氧化物对应水化物的酸性比Z的强 |
| C、Y的非金属性比X的强 |
| D、Y与Z形成的化合物是形成酸雨的主要物质 |
下列关于稀有气体的叙述不正确的是( )
| A、各原子轨道电子均已填满 |
| B、其原子与同周期ⅠA、ⅡA族阳离子具有相同的核外电子排布 |
| C、化学性质非常不活泼 |
| D、同周期中第一电离能最大 |
将铁屑溶于过量的盐酸后,再加入下列物质,会有三价铁生成的是( )
| A、硫酸 | B、磷酸 |
| C、硝酸锌 | D、氯化铜 |