题目内容
将铁屑溶于过量的盐酸后,再加入下列物质,会有三价铁生成的是( )
| A、硫酸 | B、磷酸 |
| C、硝酸锌 | D、氯化铜 |
考点:铁的化学性质
专题:几种重要的金属及其化合物
分析:铁屑溶于盐酸后,溶液中主要是H+、Cl-、Fe2+,若要将Fe2+变为Fe3+,需要强氧化性物质.
解答:
解:二价铁离子变为三价铁离子发生了氧化反应,应加入氧化性的物质,在H+存在的情况下,NO3-表现强氧化性,发生反应:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O;硫酸必须是浓硫酸才有强氧化性,稀硫酸没有氧化性;磷酸不具有氧化性;Cu2+氧化性很弱,不能氧化二价铁离子,
故选:C.
故选:C.
点评:本题考查了铁及其化合物的性质,熟悉氧化还原反应的规律是解题关键,需要注意的是在H+存在的情况下,NO3-表现强氧化性.

练习册系列答案
相关题目
为证明某可溶性一元酸(HX)是弱酸,某同学设计了如下实验方案,其中不 合理的是( )
| A、室温下,测0.1 mol/L HX溶液的pH>1,证明HX是弱酸 |
| B、室温下,将等浓度等体积的盐酸和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 |
| C、室温下,测1 mol/L NaX的pH,若pH>7,证明HX是弱酸 |
| D、在相同条件下,对0.1 mol/L的盐酸和0.1 mol/L的HX溶液进行导电性实验,若HX溶液灯泡较暗,证明HX为弱酸 |
分类是化学研究的重要方法,下列各组物质的分类正确的是( )
| A、同位素:D2、H2、T2 |
| B、含极性键、由分子构成的化合物:CO2、CCl4、NH3 |
| C、非电解质:NH3、C2H5OH、Cl2 |
D、同系物: |
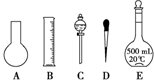
下列图所示的实验操作中,不正确的是( )
A、 滴加液体药品 |
B、 过滤 |
C、 稀释浓硫酸 |
D、 读取液体的体积 |
常温下,下列有关叙述正确的是学( )
| A、NaB溶液的pH=8,c(Na+)-c(B-)=0.99×10-6mol/L |
| B、Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、c(NH4+)=c(Cl-)的NH4Cl和氨水的混合溶液,其pH可能等于或大于7 |
| D、10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积(假设混合后的体积是两溶液体积之和)V(总)≥20mL |
 实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题: 欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫.请运用化学反应原理的相关知识研究碳及其化合物的性质.
欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫.请运用化学反应原理的相关知识研究碳及其化合物的性质.