反应2Z(g)?X(g)+Y(g),△H>0.达到平衡时,下列说法正确的是( )
| A、加入催化剂,X的产率增大 |
| B、升高温度,Y的转化率增大 |
| C、当容器活塞可活动时,充入稀有气体,平衡不移动 |
| D、充入Z气体时,Z的转化率增大 |
把3mol A与2.5mol B充入2L容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g).经5min达到平衡,生成1mol D,以C的浓度变化表示的反应速率是0.1mol/(L?min),则下列叙述中错误的是( )
| A、vA=0.15 mol/(L?min) |
| B、B的转化率为20% |
| C、B的平衡浓度是0.5 mol/L |
| D、x值等于2 |
氨氧化制硝酸,吸收塔内发生反应 3NO2(g)+H2O(l)?2HNO3(aq)+NO△H<0 要提高反应的转化率,增加浓硝酸的产量,应采取的措施( )
| A、加压 | B、加大水量 |
| C、升温 | D、减压 |
下列叙述中不正确的是( )
| A、向氯化钙溶液中通入少量CO2,有白色沉淀CaCO3生成 |
| B、向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出 |
| C、向NaAlO2溶液中通入过量CO2,有白色胶状沉淀析出 |
| D、等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下生成CO2体积比为53:42 |
根据下列三个反应方程式,判断下列关系正确的是( )
①I2+SO2+2H2O=H2SO4+2HI
②2FeCl3+2HI=2FeCl2+2HCl+I2
③2FeCl2+Cl2=2FeCl3.
①I2+SO2+2H2O=H2SO4+2HI
②2FeCl3+2HI=2FeCl2+2HCl+I2
③2FeCl2+Cl2=2FeCl3.
| A、氧化性:FeCl3>Cl2>H2SO4>I2 |
| B、还原性:SO2>HI>FeCl2>HCl |
| C、2Fe+3I2=2FeI3 |
| D、6FeI2+3Cl2=2FeCl3+4FeI3 |
下列事实能用勒夏特列原理解释的是( )
| A、H2、I2、HI平衡混合气体加压后颜色变深 |
| B、使用催化剂,提高合成氨的产率 |
| C、高锰酸钾(KMnO4)溶液加水稀释后颜色变浅 |
| D、新制的氯水在光照条件下颜色变浅 |
下列有关化学用语表示正确的是( )
| A、乙烯的结构简式为C2H4 |
| B、质子数为53,中子数为78的碘原子:53131I |
C、S2-的结构示意图: |
D、NH4Cl的电子式为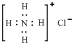 |
下列各组离子能在酸性的无色溶液中大量共存的是( )
| A、K+、Cl-、HCO3-、SO42- |
| B、Mg2+、Cl-、Al3+、SO42- |
| C、Ca2+、Fe3+、Na+、NO3- |
| D、Ba2+、Cl-、Na+、CO32- |
下列说法中,不正确的是( )
| A、相对分子质量相同,组成元素的百分含量相同的不同有机物一定是同分异构体的关系 |
| B、碳原子数相同、结构不同的烷烃一定是互为同分异构体关系 |
| C、两有机物互为同系物,则它们也是互为同分异构体关系 |
| D、碳原子数≤10的烷烃,其一氯代物没有同分异构体的烷烃有4种 |