题目内容
反应2Z(g)?X(g)+Y(g),△H>0.达到平衡时,下列说法正确的是( )
| A、加入催化剂,X的产率增大 |
| B、升高温度,Y的转化率增大 |
| C、当容器活塞可活动时,充入稀有气体,平衡不移动 |
| D、充入Z气体时,Z的转化率增大 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、催化剂只能改变反应速率,不影响平衡移动;
B、反应物有转化率;
C、反应前后气体体积相等,体积变化不会影响平衡移动;
D、反应前后气体体积不变,充入Z新平衡与原平衡等效.
B、反应物有转化率;
C、反应前后气体体积相等,体积变化不会影响平衡移动;
D、反应前后气体体积不变,充入Z新平衡与原平衡等效.
解答:
解:A、催化剂不影响平衡移动,故A错误;
B、生成物无所谓转化率,故B错误;
C、反应前后气体体积相等,体积变化不会影响平衡移动,故C正确;
D、反应前后气体体积相等,充入Z新平衡与原平衡等效,故D错误;
故选C.
B、生成物无所谓转化率,故B错误;
C、反应前后气体体积相等,体积变化不会影响平衡移动,故C正确;
D、反应前后气体体积相等,充入Z新平衡与原平衡等效,故D错误;
故选C.
点评:本题考查了催化剂对反应的影响、反应物才有转化率、影响平衡移动的因素,题目难度中等.

练习册系列答案
相关题目
下列关于摩尔质量的叙述正确的是( )
| A、1molH2SO4的质量是98g/mol |
| B、CO2的摩尔质量等于CO2的相对分子质量 |
| C、1mol任何物质的质量等于该物质的相对分子质量 |
| D、Na的摩尔质量是23g/mol |
下列有关说法正确的是( )
| A、放热反应在任何条件都能自发进行 |
| B、应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| C、任何能使熵值增大的过程都能自发进行 |
| D、△H>0,△S<0的化学反应一定能自发进行 |
关于如图所示各装置的叙述中,正确的是( )
A、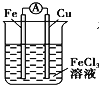 是原电池,总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
B、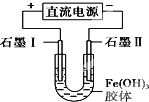 通电一段时间后石墨Ⅱ电极附近溶液红褐色加深 |
C、若用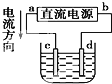 精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
D、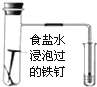 研究的是金属的析氢腐蚀,Fe上的反应为Fe-2e-=Fe2+ |
下列事实能用勒夏特列原理解释的是( )
| A、H2、I2、HI平衡混合气体加压后颜色变深 |
| B、使用催化剂,提高合成氨的产率 |
| C、高锰酸钾(KMnO4)溶液加水稀释后颜色变浅 |
| D、新制的氯水在光照条件下颜色变浅 |
设NA代表阿伏加德罗常数的数值,下列说法不正确的是( )
| A、36g镁在足量的二氧化碳气体中完全燃烧共转移的电子数为3NA |
| B、1L 1mol?L-1的Na2CO3溶液中含有Na+的数目为NA |
| C、标准状况下,2.24L CO2和SO2混合气体中含有的氧原子数目为0.2NA |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现不同的性质.下列各项的事实不能说明上述观点的是( )
| A、甲苯能使酸性高锰酸钾溶液褪色,而甲基环己烷不能使酸性高锰酸钾褪色 |
| B、乙烯能与溴水发生加成反应,而乙烷不能发生加成反应 |
| C、苯酚与溴水可直接反应,而苯与液溴反应则需要铁作催化剂 |
| D、苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应 |
下列判断不合理的是( )
| A、能电离出H+的物质不一定是酸 |
| B、蔗糖、碳酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、根据分散系中分散质粒子直径大小将分散系分为溶液、胶体和浊液 |
| D、焰色反应是化学变化 |