题目内容
氨氧化制硝酸,吸收塔内发生反应 3NO2(g)+H2O(l)?2HNO3(aq)+NO△H<0 要提高反应的转化率,增加浓硝酸的产量,应采取的措施( )
| A、加压 | B、加大水量 |
| C、升温 | D、减压 |
考点:化学反应速率的调控作用
专题:化学反应速率专题
分析:3NO2+H2O?2HNO3+NO△H<0,为提高NO2的转化率,增加浓硝酸的产量,平衡应正向移动,则降低温度、增大压强,减少生成物的浓度均可,以此解答.
解答:
解:A.增大压强,平衡正向移动,转化率增大,故A正确;
B.加大水量,纯液体基本不影响反应速率,故B错误;
C.该反应为放热反应,升温平衡逆向移动,转化率减小,故C错误;
D.减压,平衡逆向移动,转化率减小,故D错误.
故选A.
B.加大水量,纯液体基本不影响反应速率,故B错误;
C.该反应为放热反应,升温平衡逆向移动,转化率减小,故C错误;
D.减压,平衡逆向移动,转化率减小,故D错误.
故选A.
点评:本题考查化学平衡移动及转化率,明确温度、压强对反应的影响即可解答,注意把握反应为放热反应及气体体积减小的特点,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
下列各项叙述中不正确的是( )
| A、10℃时NaCl溶解度为35.7g,则此时饱和NaCl 溶液的质量分数小于35.7% |
| B、向Na2CO3溶液中加入少量NaHCO3 固体,溶液pH 减小 |
| C、50mL1.0mol?L-1盐酸与60mL 1.0 mol?L-1盐酸分别跟50mL 1.1mol?L-1NaOH溶液进行反应,中和热数值不相等 |
| D、一定条件下,向水中加入少量NaHSO4,可使水的电离程度减小 |
在反应2FeCl3+Fe=3FeCl2中,被氧化的元素和氧化剂分别是( )
| A、Fe和Fe |
| B、Cl和FeCl3 |
| C、Fe和FeCl3 |
| D、Cl和Fe |
下列化学反应的离子方程式书写正确的是( )
| A、将少量金属钠放人冷水中:Na+2H2O═Na++2OH-+H2↑ |
| B、将铝片加入烧碱溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
| C、向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+═SO2↑+H2O |
| D、向澄清石灰水中通入过量二氧化碳:CO2+Ca2++2OH-═CaCO3↓+H2O |
下列有关化学用语表示正确的是( )
| A、乙烯的结构简式为C2H4 |
| B、质子数为53,中子数为78的碘原子:53131I |
C、S2-的结构示意图: |
D、NH4Cl的电子式为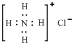 |
从碘水中提取碘可供选择的试剂是( )
| A、苯、酒精 |
| B、汽油、酒精 |
| C、汽油、乙酸 |
| D、四氯化碳、苯 |
下列有关摩尔的使用正确的是( )
| A、1mol O的质量为16g?mol-1 |
| B、0.5mol He约含有6.02×1023个电子 |
| C、2H既表示2个氢原子又表示2mol氢原子 |
| D、每摩尔微粒均含有6.02×1023个原子 |
在无色透明的溶液中可以大量共存的离子组是( )
| A、H+、K+、Fe2+、NO3- |
| B、OH-、Cl-、Na+、Mg2+ |
| C、Al3+、K+、Cl-、NO3- |
| D、Cu2+、NO3-、OH-、Cl- |