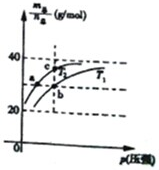
 已知N2O4(g)?2NO2(g)△H>0且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )
已知N2O4(g)?2NO2(g)△H>0且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )| A、平衡常数K(a)=K(b)<K(c) | ||
| B、反应速率:va<vb | ||
| C、温度:T2>T1 | ||
D、当
|
在反应2FeCl3+Fe=3FeCl2中,被氧化的元素和氧化剂分别是( )
| A、Fe和Fe |
| B、Cl和FeCl3 |
| C、Fe和FeCl3 |
| D、Cl和Fe |
T℃时在2L密闭容器中使x(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2(T2>T1)时,Y的体积分数(或Y的物质的量分数)与时间的关系如图2所示.则下列结论正确的是( )


| A、容器中发生的反应可表示为:4X(g)+Y(g)═2Z(g) |
| B、反应进行的前3min内,用x表示的反应速率V(X)=0.3mol/(L?min) |
| C、升高温度,反应的化学平衡常数K增大 |
| D、若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
关于摩尔的叙述中,正确的是( )
| A、摩尔是表示物质质量的单位 |
| B、摩尔是表示物质数量的单位 |
| C、摩尔既表示物质微粒数量,又表示物质质量双重意义的单位 |
| D、摩尔是表示物质的量的单位,每摩尔物质含有阿伏加德罗常数个微粒 |
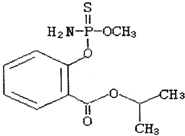 毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示,对该化合物的叙述正确的是( )
毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如图所示,对该化合物的叙述正确的是( )| A、该化合物属于芳香烃 |
| B、该化合物中至少有7个碳原子在同一平面 |
| C、该化合物的分子式为C11H14O4NPS |
| D、该化合物能发生加聚反应、水解反应和酯化反应 |
配制100mL0.100mol/LNaOH溶液时,下列操作造成浓度偏高的是①在纸上称量 ②没有冲洗玻璃棒和烧杯2-3次 ③定容时俯视刻度线 ④转移时有少量溶液溅出( )
| A、③ | B、①②③ | C、①②④ | D、②③ |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B、标准状况下,以任意比混合的氢气和一氧化碳气体共8.96L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2NA |
| C、含1 mol FeCl3的溶液中Fe3+的个数为NA |
| D、1.8 g NH4+中含有的电子数为0.1NA |
密度为1.84g/cm3,浓度为98%的浓H2SO4的物质的量的浓度为( )
| A、18.4mol/L |
| B、9.2mol/L |
| C、13mol/L |
| D、12mol/L |
下列反应既属于离子反应,又是氧化还原反应的是( )
| A、NaOH溶液与盐酸中和 |
| B、分解氯酸钾制氧气 |
| C、Zn与CuSO4 溶液的反应 |
| D、钠与水反应 |
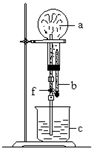 在如图装置中,烧瓶中充满干燥体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出.则a和b不可能是( )
在如图装置中,烧瓶中充满干燥体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出.则a和b不可能是( )