常温下,某溶液中水电离出的c(OH-)>1×10-7mol?L-1,则该溶液不可能的构成是( )
| A、OH-、Br-、SO42-、K+ |
| B、F-、Na+、K+、NO3- |
| C、Na+、NH4+、CH3COO-、SO42- |
| D、K+、NO3-、NH4+、Cl- |
 某种固体氧化物燃料电池是以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.则下列判断错误的是( )
某种固体氧化物燃料电池是以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.则下列判断错误的是( )| A、a极为电池负极,电极反应为:O2+4e-═2O2- |
| B、有CH4放电的b极为电池的负极 |
| C、该电池的总反应为:CH4+2O2=2H2O+CO2 |
| D、b极对应的电极反应为:CH4-8e-+4O2-═CO2+2H2O |
有关3BrF3+5H2O═HBrO3+Br2+9HF+O2↑反应的叙述中,正确的是( )
| A、还原剂和氧化剂的物质的量之比为5:3 |
| B、HBrO3和HF是还原产物 |
| C、生成1molO2,转移4mol电子 |
| D、BrF3既是氧化剂,又是还原剂 |
某温度下,在2L的恒容密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g);△H=-92.2KJ/mol,测得如下表所示的实验数据:
下列说法正确的是( )
| 物质的量(n) 时间(h) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.2 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
| A、0h~1h内N2的平均反应速率为0.1mol?L-1?h-1 |
| B、反应达到平衡时,N2的转化率小于H2的转化率 |
| C、若降低表中所示平衡体系的温度,当反应再次达到平衡后,混合气体的密度减小 |
| D、若在表中所示平衡体系中再加入N2、H2、NH3各1mol,化学平衡向正反应方向移动 |
下列关于命名的说法中错误的是( )
| A、所有烃类的命名都应选择含碳原子最多的链作主链,即“最多”原则 |
| B、二甲苯可以以邻、间、对这种习惯方法进行命名 |
| C、二甲苯也可以用系统方法进行命名 |
| D、化学式是C8H10的苯的同系物有4种同分异构体 |
下列各组物质中,互为同系物的是( )
A、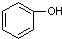 与 与 |
B、 与 与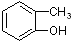 |
| C、CH3Cl与CH2Cl2 |
| D、甲醇与乙二醇 |
已知反应3Cl2+6NaOH═5NaCl+NaClO3+3H2O,下列说法不正确的是( )
| A、Cl2既是氧化剂又是还原剂 |
| B、被氧化的氯原子数是被还原的氯原子数的5倍 |
| C、氧化剂和还原剂的质量比是5:1 |
| D、NaCl是还原产物,NaClO3是氧化产物 |
如图所示,关于该装置的下列叙述中,不正确的是( )
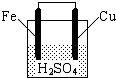

| A、铁棒是负极,发生氧化反应 |
| B、铜棒上有气体放出 |
| C、电流从锌片经导线流向铜片 |
| D、电池总反应方程式可表示为:Fe+2H+=Fe2++H2↑ |
下列关于溶液中离子的说法正确的是( )
| A、0.1 mol?L-1的Na2CO3溶液中离子浓度关系:c (Na+)=2c (CO32-)+c (HCO3-)+c (H2CO3) |
| B、0.1 mol?L-1的NH4Cl和0.1 mol?L-1的NH3?H2O等体积混合后溶液中的离子浓度关系:c (Cl-)>c (NH4+)>c (H+)>c (OH-) |
| C、常温下,醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中,离子浓度关系:c (Na+)>c (CH3COO-) |
| D、0.1 mol?L-1的NaHS溶液中离子浓度关系:c (OH-)=c (H+)-c (S2-)+c (H2S) |
T℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.则下列结论错误的是( )
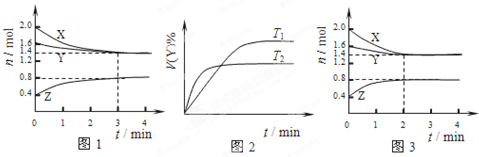

| A、容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) |
| B、反应进行前3min内,用X表示的反应速率v(X)=0.1mol/(L?min) |
| C、若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
| D、保持其他条件不变,升高温度,化学平衡向逆反应方向移动 |